ミノキシジルの中毒リスクはどれくらいなのか?

しかし、Loniten®の添付文書ではBoxed Warningが掲載されています。これはFDA(米国食品医薬品局)の指示により記載される警告文で、重篤な副作用を起こす危険性を最も強く警告するものです。 外用薬としての開発にはこの非常に強い主作用と副作用とを逆転させ開発された経緯が伺えます。先の文献のような報告があると、動物を用いた試験をしていないことは、後々こうして人と動物の社会にとってリスクにもなるということも言えるかもしれません。
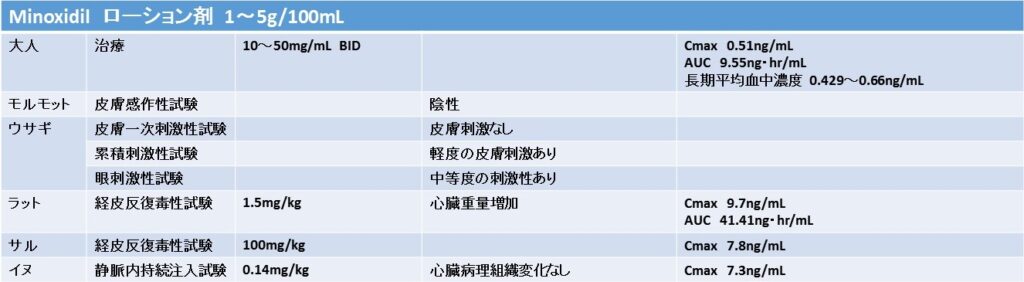
国内承認されている外用ミノキシジルの申請情報によると、用量変更による申請の内容からですが、非臨床安全性試験に関しては、モルモット皮膚感作性試験、ウサギ皮膚一次刺激性試験、累積刺激性試験、眼刺激性試験、ラット経皮反復毒性試験、サル経皮反復毒性試験が実施されており、イヌを用いた安全性試験は実施されていませんでした。外用薬としての申請ですので、経口投与毒性に関しては試験されていなくてもおかしくありません。妥当なものと考えられますし、心臓に対する作用が最も重要であることも認識されていました。
薬物動態に関する試験としてはイヌの持続静注試験が行われ、0.14mg/kgの用量で静脈内に投与されていましたが、病理組織学的な変化はないということでした。
経口ミノキシジルではどうでしょうか。ラット、イヌ、ミニブタ、サルでの経口投与試験と、ウサギの経皮局所投与試験が行われていました。こちらのイヌへの経口投与量は0.5~20mg/kgでした。この用量では、数日以内の乳頭筋/心内膜下壊死、出血性病変(右心房)、限局性心外膜炎が起こりますが、他のβアドレナリン受容体作動薬、末梢拡張薬でも同様に起こる病変と考えられていました。また長期の投与によって、慢性増殖性心外膜炎、漿液血性心膜液、心肥大および心拡大が起こりますが、慢性的な影響と考えられています。

 JALAM学術集会委員会
JALAM学術集会委員会