- トップ
- コラム一覧
コラム の記事一覧

新型コロナウイルス感染症研究における3Rs(in WC11)
The 11th World Congress on Alternatives and Animal Use in the Life Sciences(第11回 国際代替法学会;WC11)は2020年8月にオランダのマーストリヒトで開催する予定だったのですが、コロナの影響で2021年8月に順延されました。
2020年のWC11の開催は無くなりましたが、代わりにタイトルのウェビナー(https://wc11maastricht.org/webinar/)が無料で開催されることになりました。非常に興味深い内容ですし、YouTubeにアーカイブされており日本語(自動翻訳)の字幕を出すことも可能ですので、興味のある方は是非ご覧ください。個人的には2日目のジョンズホプキンス大学CATT(動物実験代替法センター)の方の講演が新型コロナ研究をゴールドラッシュのように例えていて面白かったです。
しかし代替法はあくまで他の試験を代替するものであり、今回の新型コロナウイルスなど試験自体が確立していないもの(動物実験もゴールドスタンダードと言われるものが確立していないもの)に対しては難しいということが明らかになってしまいました。もちろんiPS細胞などin vitroの試験を用いて研究していくことは必要ですが、スピード感が求められている中では動物実験と同時並行で進めていかざるを得ないのが現状です。この中でも私たちのような管理者が出来ることは、非常にシビアな感染実験などに対し、人道的エンドポイントを積極的に適用するなどのRefinementの実践だと考えています。

【Webinar】マウスの環境エンリッチメントと老齢モデルコロニーの維持(EPトレーディング株式会社提供)
実験動物の特殊飼料やエンリッチメント、水分・栄養補給用ジェルなどを取り扱っているEPトレーディング株式会社(https://www.eptrading.co.jp/index.html)に、JALAMのために日本語字幕付きWebinar動画をご提供いただきました。

AALAS(米国実験動物学会)2020で行った、ジャクソンラボラトリー Dr.Schile による「環境エンリッチメントと繁殖」、「老齢モデルコロニー の維持」の解説ビデオ(51分)
https://www.eptrading.co.jp/service/ssp/video.html

動物福祉の評価ツールのご紹介-1
〜AVMA主催の“学生動物福祉状況の評価コンテスト”〜
さて、イリノイ大のニュースによると、このコンテストの目的は、「農業、研究、伴侶など、人間のために使用される動物に影響を与える福祉問題の理解と認識を高めるための教育ツールを経験することであり、倫理的推論に対する理解の上に、科学的理論とデータに基づいた動物福祉の客観的評価を促し、批判的思考を促進し、コミュニケーション能力を向上させる」ことです。参加対象は、3・4年学部生、獣医学部生、院生(1チーム3-5人)であり、動物看護師やAVMA会員の獣医師も少数に限り参加できます(ただし、コンテストの対象外)。参加者はいくつかのシナリオに沿って出題される動物とその福祉状況を分析して、その中から優れたシナリオを選び出し、発表するというものです。
ニュースでは、“動物福祉のさまざまな事象をそのときどきの断片として客観的かつ定量的に評価することも可能ですが、福祉問題は連続したものであり、どのあたりで許容できるか、どのあたりが好ましいか、または許容できないかの判断は、多くの場合、倫理に基づく選択に帰着するものです。コンテストでは、問題解決へ学際的にアプローチするため、科学に基づく知識を倫理的価値観と統合することを学生に教えています”という風に審査の方法について説明しています。私たちが学生の動物福祉評価を審査するのであれば、北米でどのような基準やチェック方法に従って動物福祉が評価されているのかの具体例を知りたいところです。
今回はこのくらいにさせていただいて、次は、動物福祉評価のツールについて整理していきたいと思います。
参考文献
1) Beaver B. V. and Bayne K, Chapter 4 – Animal Welfare Assessment Considerations, Laboratory Animal Welfare, 29-38 (2014)
2) Animal welfare judging team provides unique experiential learning for students. (cited 2022. Oct.28)
3) AVMA Animal Welfare Assessment Contest. (cited 2022. Dec. 05)
生殖細胞が持つポテンシャル -乾燥状態でも失われない受精能力-
精子をフリーズドライする方法
では、ここからはフリーズドライ精子の作製から産子作出までの方法について具体的に解説していきます。まず、フリーズドライ精子の作製はどのように行うのか。その方法は意外と簡単です。生体から採取した精子は、トリス-EDTAバッファーと呼ばれる溶液に混ぜます。その後ガラスアンプルに充填し、凍結乾燥機で乾燥させるだけで完成します(図1)10。トリス-EDTAバッファーは、分子生物学研究で一般的に用いられている溶液で細胞から抽出したDNAを長期に保存することができる溶液です。精子がフリーズドライ保存できることが分かった当初は、細胞の培養に使用する溶液を用いてフリーズドライされていました。しかし、この方法では保存期間が長くなるにつれて、精子がダメージを受けてしまうことが分かりました。そこで、どうしたら精子がダメージを受けずに受精能力を持ち続けるか検討が始まります。精子が卵子と受精するには、まず精子が卵子表面に到達するための運動性が必要になります。しかし、運動性は受精後の胚の発生には関係なく、最終的に産子が誕生するためには、精子の中のDNAが正常でなければならないということに行き着きました。その結果、精子のDNAをフリーズドライした後も正常に維持する溶液を長年検討する中でトリス-EDTAバッファーの利用を思いつきました。そして、実際にこの溶液を用いて精子をフリーズドライしたところ、高い受精能力を維持できることが明らかとなりました10。さらに、精子DNAを分解する酵素は、温度上昇により活性を高めることが分かったため、フリーズドライ精子を4℃で保存したところ、分解酵素の活性を抑制することができ長期間保存することに成功しました。細胞を保存するためには、細胞を破壊するあらゆる要素から守るために多くの試薬や細胞保護物質を混ぜた溶液を作らないといけないと思っていましたが、たった2種類の試薬を含むトリス-EDTAバッファーで精子のDNAが保存できてしまったことは驚きでした。このように、精子DNAを保護してフリーズドライすることに成功しましたが、現在のフリーズドライ法では運動性を維持することができないため、水で戻した精子は、その形はきれいに維持しているものの運動性は復活できないというのが現状です。
動かないフリーズドライ精子から産子は得られるのか?
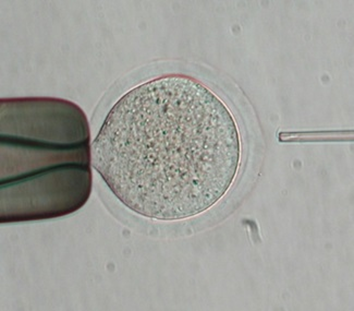
精子を卵子と受精させるには、人工受精や体外受精が用いられます。この方法は精子に運動性がないと成立しない技術であるため、水に戻した後動かないフリーズドライ精子にこの受精方法は使えません。では、どのようにフリーズドライ精子を卵子と受精させるのか。その方法は顕微授精です。顕微授精は、微細なガラス管に精子を吸引し、そのガラス管を卵子内に挿入することで受精させる技術であり、別名ICSI(Intracytoplasmic Sperm Injection;イクシー)と呼ばれる動物だけでなくヒトの不妊症治療の主力技術として利用されている技術です(図2)。ICSIは、受精の概念を大きく変えた技術であり、これまで動かない精子や運動性が極端に低い精子は受精できない精子として認識されていたのが、ICSIにより産子が誕生したことで動かない精子でも受精能力を維持していることが証明されました。さらに、ICSIを用いることで形成過程の未熟な精子からも産子を誕生させることができるようになり、体外での受精技術は革新的に進化しました。現在、多くの動物種でフリーズドライ精子から産子が得られているのも、ICSIの技術開発が大きく影響しています。
我々はこれまで、冷蔵庫で3~5年間保存したマウス・ラットのフリーズドライ精子から産子を誕生させることに成功しており、フリーズドライ精子保存法は遺伝資源を保存する技術として十分活用することができます11-12。また、マウス・ラット以外にも上述した多くの動物で成功例が報告されていることから、今後ますます利用が多くなることが予想されます。

精子はアンプルの底に粉状になる

卵子や受精卵はフリーズドライ保存できるの?
ここまで、精子のフリーズドライ保存法の実際についてご紹介してきましたが、卵子や受精卵はフリーズドライ保存できるのか疑問に思う方もいらっしゃると思います。現時点では、卵子や受精卵のフリーズドライ保存に成功したという報告はありません。卵子や受精卵は他の細胞と比べて非常に大きな細胞であるため、フリーズドライ保存が難しく成功に至っていませんが、今後の科学の進歩が期待されます。さらに、フリーズドライ精子も現在運動性を維持できていませんが、将来運動性を持つフリーズドライ精子が作製できるようになれば、顕微授精が難しい施設や動物種でも人工授精や体外受精を使って産子を誕生させられるようになるかもしれません。
最後に
フリーズドライ精子保存法は現在、動物において実用化レベルにまで開発することができていますが、まだ改良しなければならない課題もあります。しかし、これまで多くの動物種で成功例が報告されており、筆者らも精子フリーズドライ保存法の活躍の場を広げるために、この方法を絶滅危惧種の保全に応用しています13。これまでに約70種の野生動物の精子を保存しており、この中にはヤンバルクイナ、オオワシ、オジロワシ、ツシマヤマネコ、アマミノクロウサギといった国内の絶滅危惧種も含まれています。我々が開発した技術が動物を絶滅から守ることにつながってほしいと思います。
今回のコラムで、生物、細胞が持つポテンシャルを知り、少しでも興味を持っていただければ幸いです。詳しい研究内容は当研究室のHPをご覧ください1。
参考文献
1. 大阪公立大学大学院獣医学研究科実験動物学教室 https://www.omu.ac.jp/vet/las
2. Kaneko T, Sakuma T, Yamamoto T, Mashimo T. Simple knockout by electroporation of engineered endonucleases into intact rat embryos. Sci Rep. 4: 6382, 2014. doi: 10.1038/srep06382.
3. Kaneko T, Mashimo T. Simple Genome Editing of Rodent Intact Embryos by Electroporation. PLoS One. 10: e0142755, 2015. doi: 10.1371/journal.pone.0142755.
4. Kaneko T.Genome Editing in Mouse and Rat by Electroporation. Methods Mol Biol. 2637: 125-134, 2023. doi: 10.1007/978-1-0716-3016-7_10.
5. Kaneko T, Endo M, Tsunoda S, Nakagawa Y, Abe H. Simple induction of pseudopregnancy by artificial stimulation using a sonic vibration in rats. Sci Rep. 10: 2729, 2020. doi: 10.1038/s41598-020-59611-1.
6. Endo M, Tsunoda S, Tawara H, Abe H, Kaneko T. Successful pseudopregnancy of rats by short period artificial stimulation using sonic vibration. Sci Rep. 12: 1187, 2022. doi: 10.1038/s41598-022-05293-w.
7. Wake Y, Endo M, Tsunoda S, Tawara H, Abe H, Nakagawa Y, Kaneko T.Successful induction of pseudopregnancy using sonic vibration in mice. Sci Rep. 13: 3604, 2023. doi: 10.1038/s41598-023-30774-x.
8. Kaneko T. Simple gamete preservation and artificial reproduction of mammals using micro-insemination techniques. Reprod Med Biol. 14, 99-105, 2015. doi: 10.1007/s12522-014-0202-4.
9. Kaneko T. Sperm freeze-drying and micro-insemination for biobanking and maintenance of genetic diversity in mammals. Reprod Fertil Dev. 28, 1079-1087, 2016. doi: 10.1071/RD15386.
10. Kaneko T. Simple sperm preservation by freeze-drying for conserving animal strains. Methods Mol Biol. 1239, 317-329, 2015. doi: 10.1007/978-1-4939-1862-1_19.
11. Kaneko T, Serikawa T. Long-term preservation of freeze-dried mouse spermatozoa. Cryobiology 64, 211-214, 2012. doi: 10.1016/j.cryobiol.2012.01.010.
12. Kaneko T, Serikawa T. Successful long-term preservation of rat sperm by freeze-drying. PLoS One 7, e35043, 2012. doi: 10.1371/journal.pone.0035043.
13. Kaneko T, Ito H, Sakamoto H, Onuma M, Inoue-Murayama M. Sperm preservation by freeze-drying for the conservation of wild animals. PLOS ONE. 9, e113381, 2014. doi: 10.1371/journal.pone.0113381.
コラム 実験動物

動物実験従事者におけるCompassion Fatigueの分類(ProQOLを用いた分類)
Compassion Fatigueに対処する上で、最も重要なのは自分が今どのような状態にあるかを認識することです。その認識を手助けする分類方法として、Professional Quality of Life (ProQOL)というものがあります。
ProQOLは、相手と自らの職務との関連で感じるQOLの事と定義されており、ネガティブ・ポジティブの両側面を含むものとして概念化されています。つまり、相手がいる仕事において、ポジティブな方向に振れればそれはCompassion Satisfaction(共感満足:CS)であるし、ネガティブな方向に振れればそれはCompassion Fatigue(共感疲労、思いやり疲労:CF)であるとしています。さらにCFを2つに分類することができ、一般的にその仕事を続けられないと思えばそれはバーンアウト(燃え尽き症候群)であるし、その仕事を続けたいと思えば二次的外傷性ストレスだとされています。このようなProQOLを模式図化したものが以下の図です。
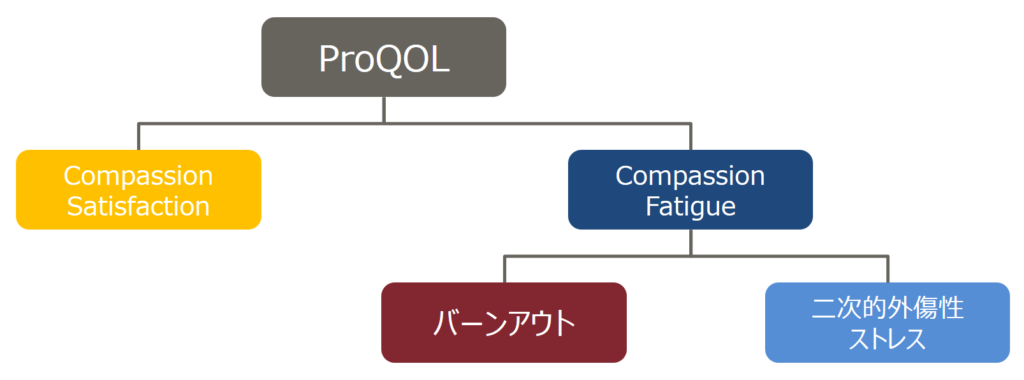
ProQOLは現在第5版が発行されていますが、日本語訳されたものは第4版が最新のものになっています(https://img1.wsimg.com/blobby/go/dfc1e1a0-a1db-4456-9391-18746725179b/downloads/Japanese.pdf)。第4版では30項目の問いから構成されており、その問いに対して0~5の6段階(0=まったくない、1=めったにない、2=たまにある、3=ときどきある、4=よくある、5=とてもよくある)でどの頻度で当てはまるかを数値化していき、その合計点で判断するといったものです。では具体的に項目を見ていきましょう。なお、項目は私の方で実験動物従事者用(特に飼育管理の方向け)にアレンジがしてありますので、公式なものではないことを申し添えておきます。

続いて自己採点方法です。
CSの平均点は37点です。上位約25%の人が42点以上、また下位25%は33点以下の得点です。42点以上であれば現在の仕事によってかなりの職業的満足感が得られていると考えられますが、33点以下であれば現在の仕事に問題を抱えているか、もしくは仕事以外の活動から満足感を得ているなど、他に理由がある場合も有ります。
バーンアウトの平均点は22点です。上位25%の人が27点以上、また下位25%は18点以下の得点です。18点以下であれば自身の業務遂行能力に関して肯定的な気持ちを持っていることを反映していますが、27点以上であれば効果的に自分の役割を果たせないのは仕事のどういった部分であるかについて省みたくなるかもしれません。
二次的外傷性ストレスの平均値は13点です。上位25%の人が17点以上、また下位25%は8点以下の得点です。17点以上の場合、仕事のどういう部分が恐怖感を与えているのかについてじっくり考える時間を持つことも良いかもしれません。高得点が必ずしも問題があることを意味するわけではありませんが、今の仕事や職場環境についてどう感じているのかを考察してみる方が良いのではないかという事を示唆しています。
今回の平均値などの得点はあくまでProQOLの基準であり、動物実験従事者に対してチューニングされたものではありません。ちなみに私はどの項目も平均点付近でしたので、どれにも合致しないといったごく普通の感じでしょうか。こちらは日本人と外国人である場合も結果が異なるでしょうし、飼育管理業務が主体的なのか、実験作業が主体的なのかによっても異なるかもしれません。いずれにせよ、このProQOLの概念が広がり、多くの方が実施することで信頼性が高まっていくと考えられますので、是非みなさんも実践して頂ければと思います。

動物福祉の評価ツールのご紹介-2
〜福祉を評価するツールを紹介するサイト1:USDAのNational Agricultural Library〜
Welfare Assessment Training and Resources(動物福祉の評価のトレーニングとリソース)
1)”CCAC Guidelines: Animal Welfare Assessment“
カナダ動物愛護協議会(CCAC, Canadian Council on Animal Care)が2021年に作成したガイドラインへのリンクです。このガイドは、なぜ福祉を評価するのか、福祉指標を特定し、福祉評価の文書化について説明しています。このガイドラインの要点を、極端に短くまとめれば、以下の5点に集約できます。
・評価の監督は委員会が担うが、評価そのものは評価実施者に任せる
・動物は健康であるべき
・福祉評価は定期的に実施する
・評価に用いた情報は研究者などが利用できるよう記録する
・評価の結果を動物実験委員会は利用する
2)“Welfare Assessment”
“動物実験の3Rsの推進”を図る、英国NC3Rs(The National Centre for the Replacement, Refinement & Reduction of Animals in Research)が作成した“Welfare Assessment”ガイドにリンクしています。このガイドでは、以下の情報を提供しています。
・福祉指標の特定
・実際上の侵襲性の評価と報告
・効果的な記録の保持とレビュー
・スタッフのトレーニング
・関連リソース
3)“Guide to Welfare Assessment Protocols”
苦痛の軽減(Refinement)に関する英国合同ワーキンググループ(JWGR)が2011年、Laboratory Animals誌に発表した“A guide to defining and implementing protocols for the welfare assessment of laboratory animals: eleventh report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement” へのリンクです。このガイドには、動物の苦痛の軽減に関する事項がかなり細かく記載されています。
・効果的な福祉評価スキームのための一般原則
・チームアプローチ
・良好な福祉の定義
・適切な福祉指標の選択
・動物福祉指標の記録システム
・評価のタイミング・期間・頻度
・実践的な福祉評価(観察・潜在的な福祉問題の指摘)
・福祉記録の確認
・倫理・動物愛護委員会との連携
・さらなる情報へのアクセス

動物の難治性疾病に対する創薬研究 〜動物の免疫療法について〜
3. イヌの腫瘍疾患に対する創薬研究
イヌの死因の約3割は悪性腫瘍(がん)であるとされており、特に高齢犬ではその傾向が高いです。イヌの腫瘍に対しては現在、外科療法・放射線療法・化学療法の3大療法が主として用いられていますが、高齢犬の体への負担や副作用、がん種と療法との相性などの面で制限を受ける場合も多く、3大療法に加えて新たな治療戦略の開発が望まれています。我々はまず、イヌにおいても、悪性黒色腫や血管肉腫、肥満細胞腫等を中心とした数々の悪性腫瘍においてPD-L1 が高発現していること、またこれに対する抗PD-L1 モノクローナル抗体を用いてその免疫抑制機序を遮断するとイヌ免疫担当細胞の機能を回復できることを明らかにしました(Maekawa et al., PLoS One. 2014. 9(6):e98415. Maekawa et al., PLoS One. 2016. 11(6):e0157176)。そこで、イヌの腫瘍治療に応用できる免疫チェックポイント阻害薬としてイヌ用の抗PD-L1抗体医薬品を開発し、難治性の悪性腫瘍に罹ったイヌに対する臨床応用研究を北海道大学動物医療センター高木 哲准教授(現麻布大学・教授)と行いました。その結果、悪性黒色腫と未分化肉腫に罹ったイヌの一部で、明らかな腫瘍の退縮効果が確認され、さらに悪性黒色腫では肺に転移した後の生存期間を延長する効果も得られました。
● 2017年8月25日:イヌのがん治療に有効な免疫チェックポイント阻害薬(抗PD-L1 抗体)の開発にはじめて成功~北海道大学動物医療センターにおける臨床研究成果~
(https://lab-inf.vetmed.hokudai.ac.jp/content/files/Research/2017.8.25_jyu.pdf)
● New therapeutic antibody for dog cancers
(https://www.global.hokudai.ac.jp/blog/new-therapeutic-antibody-for-dog-cancers/)
さらに、肺に転移した悪性黒色腫をもつイヌ 29 頭(ステージ4 (末期がん))に対し、抗 PD-L1 抗体による試験的治療を行ったところ、イヌで肺転移巣を含む腫瘍の退縮が観察されたほか、北海道大学動物医療センターにおいて治療した過去の症例と比べ、抗 PD-L1 抗体治療群では有意に生存期間が長いことが明らかになりました。
● 2021年2月15日:続報・肺転移のあるイヌ悪性黒色腫に抗PD-L1抗体が有効であることをはじめて実証 ~イヌ用免疫チェックポイント阻害薬の実現に大きく前進~
(https://www.hokudai.ac.jp/news/pdf/210215_pr.pdf)
● New therapy target for malignant melanomas in dogs
(https://www.global.hokudai.ac.jp/blog/new-therapy-target-for-malignant-melanomas-in-dogs/)
しかし、奏効(がんの退縮効果)が得られるイヌは一部にとどまっていました。そこで、それまでに抗 PD-L1 抗体による治療を行った肺転移のある口腔内悪性黒色腫のイヌについて回顧的な解析を行うことで、放射線療法と抗 PD-L1 抗体療法の組み合わせがより良い治療効果に繋がるかを検討しました。その結果、放射線治療歴の有無やそのタイミングが抗 PD-L1 抗体の治療効果と相関することを発見しました。すなわち、「RT(放射線療法)なし群」では、20頭中2頭で肺転移病変が抗 PD-L1 抗体治療に反応し(完全奏効1頭及び維持1頭)、 臨床的有用率は 10.0%でしたが、「RT 前治療群」では、9頭中4頭で完全奏効及び1 頭で維持/部分奏効が認められ、肺転移病変の臨床的有用率は55.6%となり、これは 「RT なし群」と比較して有意に高い比率(P = 0.016)であることを確認しました。この組み合わせ療法において安全性にも大きな問題は認められなかったことから、 放射線治療を免疫チェックポイント阻害薬の開始前に適用することで、 より良い治療効果が得られる新しい治療法となる可能性があります。本臨床研究の成果は、放射線療法が適用される他のがんにも適用できる可能性があり、免疫チェックポイント阻害薬の適用拡大と併せて検討を進めることでイヌの腫瘍に対するより良い治療の提供に繋がるものと期待されます。
● 2023年6月2日:イヌ悪性黒色腫に対して放射線治療との併用で抗PD-L1抗体の効果が高まることをはじめて報告 ~イヌ用免疫チェックポイント阻害薬のより良い使用法の実現に期待~
(https://www.hokudai.ac.jp/news/pdf/230602_pr.pdf)
● Combination therapy effective against canine melanoma – Hokkaido University
(https://www.global.hokudai.ac.jp/news/8896)
さらに、これまで臨床研究の対象としてきた口腔内悪性黒色腫以外の、進行した悪性腫瘍に罹患したイヌ 12 頭に対して、抗PD-L1 抗体の安全性と有効性を調べるための臨床研究を行いました。その結果、鼻腔内腺癌の 1 頭及び骨肉腫の 1 頭で腫瘍の退縮が認められました。
● 2023年10月5日:イヌの鼻腔内腺癌や骨肉腫に免疫チェックポイント阻害剤が有効であることを初めて報告 ~イヌ用抗PD-L1抗体による免疫療法の適用拡大に期待~
(https://www.hokudai.ac.jp/news/pdf/231005_pr.pdf)
抗 PD-L1 抗体治療単独での効果は限定的であり、治療効果を高めるための併用療法の開発が求められていることは先述のとおりです。そこで次に、抗 PD-L1 抗体治療に併用する免疫療法薬として、イヌ Cytotoxic T lymphocyte Antigen-4(CTLA-4)に対する阻害抗体(抗 CTLA-4 抗体)を新たに開発しました。そこで抗 PD-L1 抗体単独治療を行ったものの腫瘍の拡大認められたイヌに対して抗 CTLA-4 抗体による併用療法を行いました。その結果、抗腫瘍効果の評価が可能だった 6 頭のうち、1 頭で腫瘍の退縮が認められました。本研究成果は、抗 PD-L1 抗体単独治療に効果を示さなかったイヌにおいても、抗 CTLA-4 抗体との併用治療による免疫療法が有効となる可能性を示しており、イヌ腫瘍に対する新たな免疫療法の実現につながる重要な知見となります。
● 2025年5月20日:イヌのがんに抗 CTLA-4抗体治療が有効であることを初めて報告 ~イヌのがんへの免疫療法の適用拡大に期待~
(https://www.hokudai.ac.jp/news/pdf/250520_pr2.pdf)
これらの研究開発品は,悪性黒色腫をはじめとしたイヌの難治性腫瘍の治療薬として期待できる成果と考えられ、現在も北海道大学動物医療センターにて臨床研究を継続実施中です(図3)。

● https://www.vetmed.hokudai.ac.jp/VMTH/aboutus/research/
コラム 創薬研究

安楽死にまつわる諸問題
欧米と異なる日本独自の宗教観と言う観点から、日本人に特有の安楽死に抱いている感情や作法を振り返る
動物実験従事者におけるCompassion Fatigueについて解説する
コラム 動画

動物実験におけるPAM(Post Approval Monitoring)
動物実験は申請後に動物実験委員会等で承認され、実験を実施し、終了報告によって終了するといった一連の流れがあります。終了報告では申請時から逸脱した操作は無かったとか、申請時の使用予定匹数を超過するものではなかったなどの報告をしますが、それらが実際に報告通り行われていたかを知るすべが少ないのが現状です。そこで考えられたのがPAM(承認後モニタリング)という、実験が走っている最中に本当に申請通り行われているかを確かめるための仕組みです。
PAMは通常、動物実験委員会のメンバーや管理獣医師が行いますが、様々なタイプのものがあります。動物実験施設にふらっと入って、その場に居合わせた研究者に軽く質問をしながら何か困ったこと無い?と聞いてやりとりをするのもありますし、実験や手術などに立ち会って最初から最後まで手技についてチェックするのもあります。私は経験がありませんが、事前通告なしの抜き打ちによるPAMも存在するとのことです。

PAMを実施する際には苦痛度の高い試験や、中大動物の大規模手術、PAMを受けた経験のない人を優先して実施するところが多いようです。もちろん動物実験を実施する際には教育訓練を受講してもらいますが、何事もよくある話で、ある一定の割合で内容を理解していない人が必ず出てきます。そう言った意味でもPAMは現場でのセーフティネットの役割を果たしていると考えています。またPAMとセットで多いのが匿名の通報制度です。動物実験をする際に動物虐待があってはなりませんが、疑わしい場合があった際には匿名で通報できるようなシステムを採っています。これらの通報を受けて緊急のPAMを実施することもあります。研究の進捗はもちろん重要ですが、動物の命を扱っている以上、科学的根拠もなしに3Rsや5Freedomsを侵害してはならないからです。
PAMを実施する際には研究員からの反発も予想されますが、こと製薬企業においては品質保証、QA(Quality Assurance)の考えが根付いており、他者からチェックを受けることが日常茶飯事ですので案外スムースに実施できるといった印象です。個人で動くことの多いアカデミアなどではこう上手くはいかないかもしれません。
コラム 動物実験







