- トップ
- コラム一覧
動物実験の記事一覧

新型コロナウイルス感染症研究における3Rs(in WC11)
The 11th World Congress on Alternatives and Animal Use in the Life Sciences(第11回 国際代替法学会;WC11)は2020年8月にオランダのマーストリヒトで開催する予定だったのですが、コロナの影響で2021年8月に順延されました。
2020年のWC11の開催は無くなりましたが、代わりにタイトルのウェビナー(https://wc11maastricht.org/webinar/)が無料で開催されることになりました。非常に興味深い内容ですし、YouTubeにアーカイブされており日本語(自動翻訳)の字幕を出すことも可能ですので、興味のある方は是非ご覧ください。個人的には2日目のジョンズホプキンス大学CATT(動物実験代替法センター)の方の講演が新型コロナ研究をゴールドラッシュのように例えていて面白かったです。
しかし代替法はあくまで他の試験を代替するものであり、今回の新型コロナウイルスなど試験自体が確立していないもの(動物実験もゴールドスタンダードと言われるものが確立していないもの)に対しては難しいということが明らかになってしまいました。もちろんiPS細胞などin vitroの試験を用いて研究していくことは必要ですが、スピード感が求められている中では動物実験と同時並行で進めていかざるを得ないのが現状です。この中でも私たちのような管理者が出来ることは、非常にシビアな感染実験などに対し、人道的エンドポイントを積極的に適用するなどのRefinementの実践だと考えています。

動物実験の情報発信(イギリス編)
コミュニケーション

コミュニケーションは情報発信において非常に重要な役割を果たします。UARが設立された当初はテレビや新聞などマスメディアで動物実験擁護活動を展開していましたが、現在ではインターネットやソーシャルメディアでの発信に切り替わってきているようです。動物実験反対派の事実に異なる主張に対し、正しい情報を公開し、その意義を訴えるという姿勢を明確にしており、このことによりメンバーや組織が動物実験に改めて理解を深めることで、さらに自信をもって自らの立場を鮮明にアナウンスすることも出来るようになってきているとのことです。つまりは情報発信側のトレーニングにもなっているようですね。
また、情報開示に関する活動として、UARではweb上で動物実験施設のバーチャルツアーを開設(http://www.labanimaltour.org/)しています。
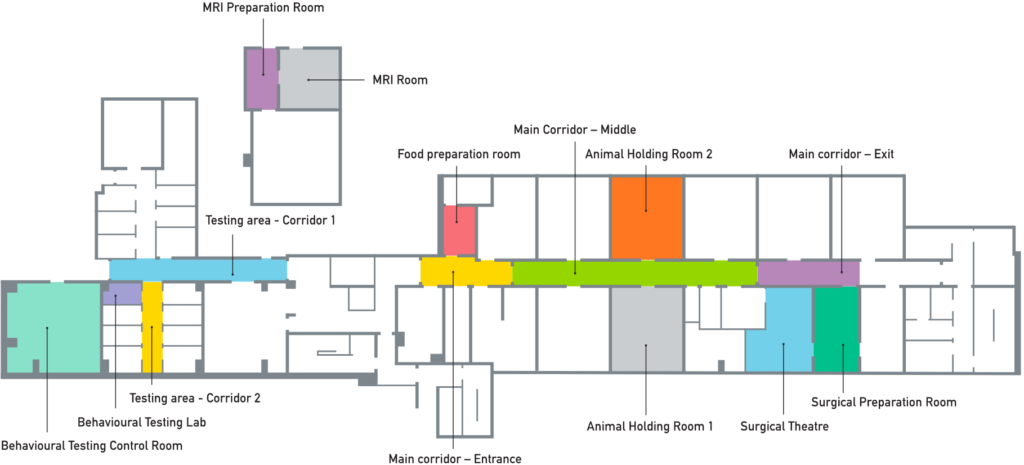

上の写真はオックスフォード大学の動物実験施設のバーチャルツアーです。公開している部屋は限られますが、色の付いている部屋はすべて見ることが出来ますし、Googleのストリートビューのように360度ぐるぐる回して見ることが出来ます。また驚くべきことに、このようにサルに電極を付けた非常にシビアな試験を公開しており、逆にオックスフォードの動物実験に対する透明性を高めるものになっています。
このようにUARの様々な活動を見てきましたが、イギリスでは長年これらの活動に取り組んできただけあって非常に洗練されたものとなっています。現在、日本でもUARの活動を見習って情報発信活動を始める動きが出てきていますが、それにはまず現在の閉鎖的な環境を打破し、胸襟を開いて、動物実験はそもそも何のために行っているのかという原点に立ち返って正しい情報発信を進めていく必要があると考えています。

人道的エンドポイント
通常、動物実験では終了時の目標を定め、その目標に到達した時点で実験を終了し安楽死処置を施します。その目標到達時点を実験のエンドポイントと呼びますが、感染症やがんなど、非常にシビアな実験では死がエンドポイントと設定されている場合が数多くあります。しかし最近では動物福祉の観点から、死をエンドポイントとするのではなく、死に繋がる兆候、もしくはこれ以上は得られる成果よりも動物の苦痛度が高いと判断される兆候が見られた時点をエンドポイントと定め、その時点で安楽死処置することで動物に不要な苦痛を与えないようにするといった考えが広がってきました。この安楽死処置するタイミングの事を人道的エンドポイント(Humane Endpoint)と呼びます。
人道的エンドポイントを少し具体的に見ていきましょう。感染症の実験は非常にシビアなものであり、一般的には生死で判断する場合が多く、縦軸に生存率、横軸に感染後の経過日数をプロットした生存曲線を描く場合があります。
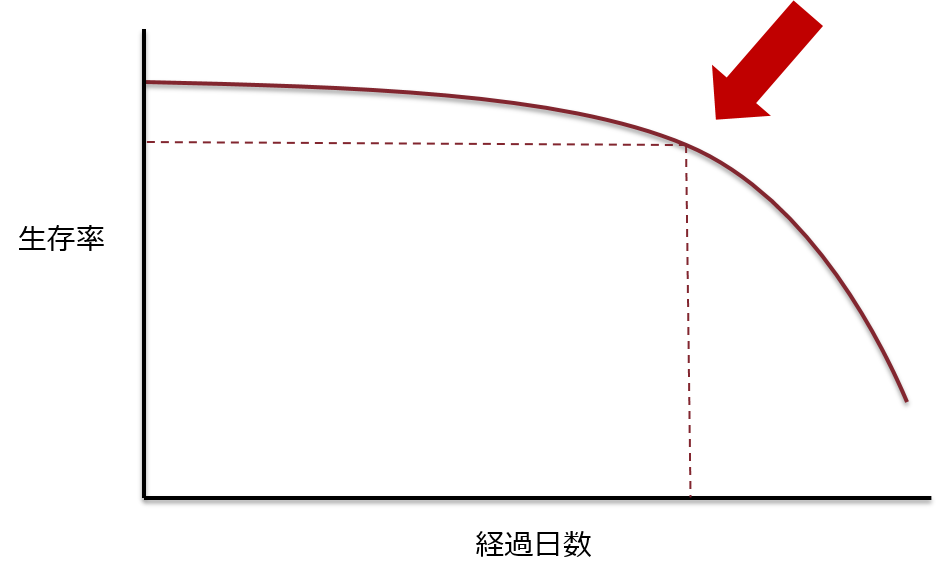
矢印の時点に注目して頂きたいのですが、このあたりから生存率が急に下がる(=死亡個体が多くなる)ことが分かります。この後の死亡に繋がる何らかの所見がこの時点、もしくはもう少し前の時点で得られれば「その所見を得た〇日後に死亡する」といったデータが得られるのです。
その所見には以下のようなものが例として挙げられます。
● 摂餌量の低下
● 体重減少
● 体温の低下
● 外貌所見(見た目の変化)
中でも外貌所見は動物の状態を非常に鋭敏に捉えることが出来ます。2010年、Nature Methodsに非常に興味深い論文が掲載されました。マウスの表情によって苦痛度を推測するといった論文です。
Langford, D., Bailey, A., Chanda, M. et al. Coding of facial expressions of pain in the laboratory mouse. Nat Methods 7, 447–449 (2010). https://doi.org/10.1038/nmeth.1455
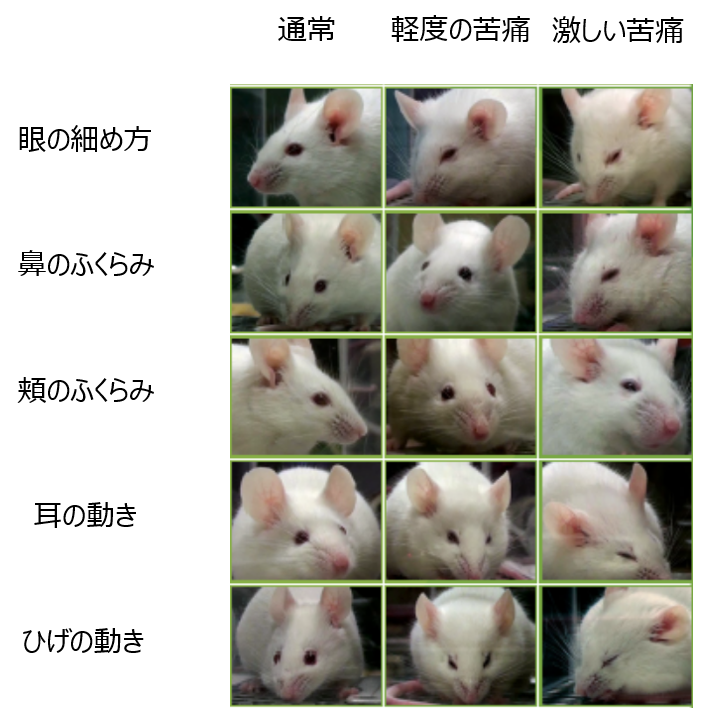
このマウスの表情はグリマススケール(しかめっ面の尺度)として知られ、現在ではマウスに限らず多くの動物で作成されています。このように動物の苦痛度を可視化し、スコア化することで各々の感覚に頼っていたものを標準化することが出来るようになってきました。これらを用いることで動物の不要な苦痛を削減すると共に実験を早期に終了することが出来、研究のスピードが増したとも言われています。
このように現在の研究現場では研究者、飼育管理担当者、管理獣医師などが協力して動物の苦痛を除去し、研究の進捗を早める努力が続けられています。
コラム動物実験

実験動物のケージサイズ
と言うのも、実験動物の分野では動物福祉を念頭に入れながら飼育することはもちろんですが、多くの科学者たちが協力し、科学的根拠に基づいてケージサイズを決定してきた背景があります。現在、米国をはじめ世界中の多くの国で採用されているイヌのILAR (Institute for Laboratory Animal Research)の基準(ILAR Guide)、そしてまだ採り入れている国は少ないものの動物福祉に先進的なEUの基準(ETS 123)は以下のとおりです。
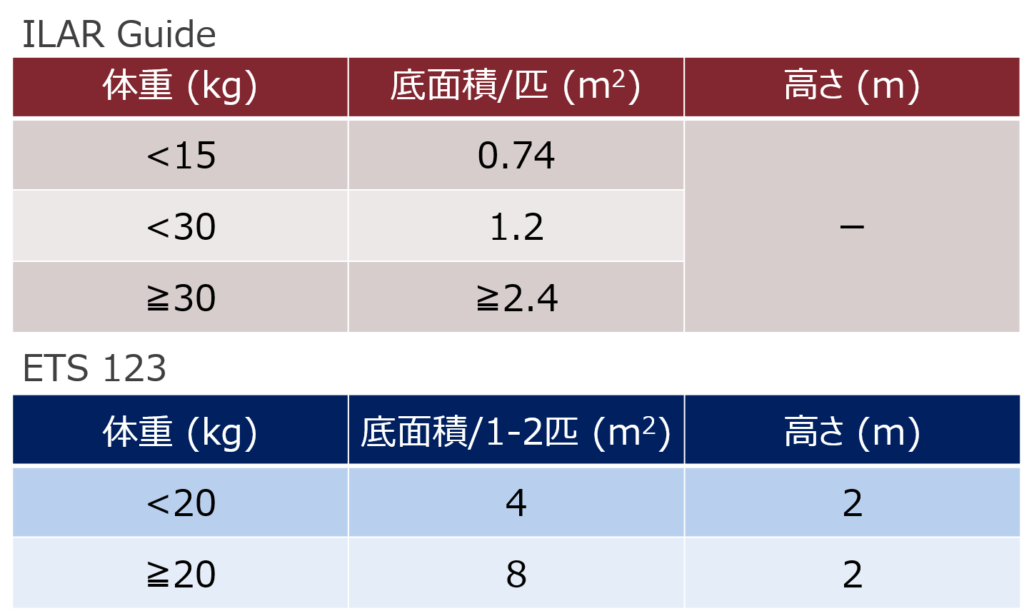
ILAR Guideは多くの改訂を経て、2011年に発行された第8版が最新のものになっています。この第8版を発行する際にはケージのサイズが大きく変更されましたが、研究者とブリーダーなどの業界団体との交渉が盛んになされた結果、こちらで落ち着いたと伺っています。その理由としてEUのように動物福祉を推進することはもっともですが、それによって実験動物が飼育できなくなり、結果的に研究の進捗が妨げられる事態は避けなければならないからです。そう言った意味で、ILARの基準は動物行動学などの科学的根拠と動物福祉の折り合いがついた結果だと考えられているため、多くの国で採用されているのだと私自身は考えています。
こういった科学的根拠なしに、かつ、業界との落としどころを見つけることなく様々な基準を決定すると、表に出てこない部分での飼育が広がる恐れがあり、結果として不幸な動物が増えてしまうのではないかと懸念しています。環境省の基準案は検討会に環境大臣が出席するほどの力の入れようですので、覆ることは恐らくないとみています。今回、このように舵を切ってしまったわけですから経過措置の期間やケージや施設の改作に関する補助など様々なサポートに関して今後議論して頂きたいと思います。
翻って我々の業界もILARサイズに収まっていればそこで飼い続けても良いのかといった問題はあるため、今回の環境省の基準案にある分離型の考えにある、定期的な運動は必要でしょうし、ゆくゆくはEUの基準での飼育が求められるものだと考えています。しかしそれには飼養数の減少が必要ですし、そのためにはイヌでの実験に代わる代替法の開発が急務であると考えています。
コラム動物実験

実験動物の安楽死方法
愛玩動物や展示動物などの終生飼育動物とは違い、実験動物は非終生飼育動物であるため、基本的には安楽死によってその生涯を終えます(里親制度除く)。動物実験従事者が守るべきガイドラインのひとつでもある、環境省の「実験動物の飼養及び保管並びに苦痛の軽減に関する基準」には安楽死に関する以下の記載があります。
実験動物管理者、実験実施者及び飼養者は、実験等を終了し、若しくは中断した実験動物又は疾病等により回復の見込みのない障害を受けた実験動物を殺処分する場合にあっては、速やかに致死量以上の麻酔薬の投与、頸(けい)椎(つい)脱臼(きゅう)等の化学的又は物理的方法による等指針に基づき行うこと。
この事を受け、各施設では独自に安楽死に対する規程を作成し実施していると思いますが、それらの規範となるものがAVMA(米国獣医学会)の安楽死に関するガイドライン(https://www.avma.org/resources-tools/avma-policies/avma-guidelines-euthanasia-animals)です。
こちらのガイドラインは実験動物に限ったものではなく、愛玩動物や産業動物など様々な分野の動物に対する安楽死方法が科学的視点から規定されています。安楽死に関しては動物が苦しむことなく死を迎える必要があり、それにはどうしても科学的根拠が必要になるため、このガイドラインは国内の各施設でも非常に重宝されています。また本ガイドラインは2020年に更新された非常に新しいものです(7年ぶりに更新)。
動物実験関係者だけでなく、動物に関わる全ての方に見て頂きたいガイドラインなのですが、いかんせん英語で全121ページという膨大な量のため足踏みしてしまう方が多いと思います。その時に参考になるのがミシガン大学のガイドライン(https://az.research.umich.edu/animalcare/guidelines/university-michigan-euthanasia-guidelines)です。
こちらはAVMAガイドラインとは異なり、イヌでCO2での安楽死が不可になっているなど若干の改変はありますが、実験動物としては現場に即したものであり、なおかつペントバルビタールなどのバルビツールによる静脈内麻酔など優先度の高い化学的安楽死方法が上に来ていることも動物に対する苦痛度を考えた上で非常に使いやすいものとなっています。
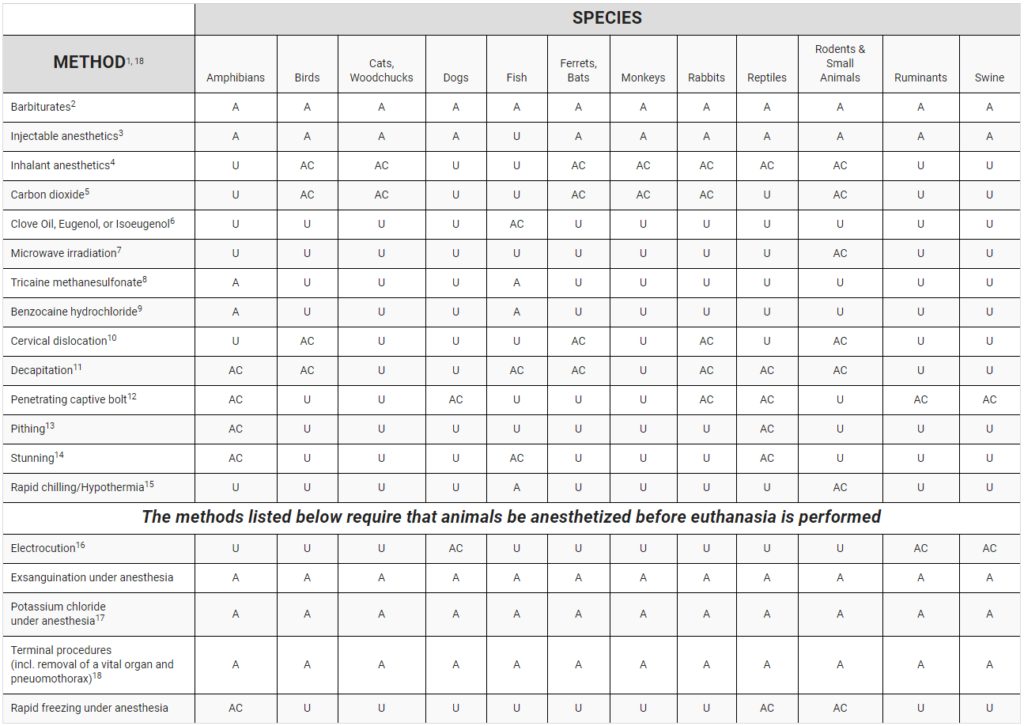
なお、表の読み方は以下のとおりです。
A = Acceptable – those which consistently produce a humane death when used as the sole means of euthanasia
AC = Acceptable with Conditions – those which consistently produce a humane death when specific conditions are met
U = Unacceptable – deemed inhumane under any conditions, or found to pose substantial risk to human applying the technique
そしてここからは非公式になりますが、私の方で勝手にこのミシガン大学の安楽死ガイドラインの表を翻訳してみました。
-1024x657.png)
安楽死に関する情報は日進月歩の状態です。前回2013年の時にはCO2での安楽死は10~30%/minでの流速で容器内の空気を置換していくと良いとされていたのですが、今回の改訂では30~70%/minで置換していく方が実は動物にとって負担が少なかったとの報告がなされています。また、魚類の安楽死も現在は化学物質による安楽死法がメインですが、2019年にヨーロッパで開催された学会では低体温での安楽死の方が苦痛が少ないことが示唆されたとの報告もされています。このように安楽死といった最後にできる実験処置としては、動物の苦痛の軽減を何よりも優先して、情報をアップデートしていく必要があると考えています。

ARRIVEガイドライン2.0が公開されました
7月14日にNC3Rs(英国3Rセンター)にてARRIVEガイドライン2.0が公開(https://arriveguidelines.org/)されました。2010年に初めて公開されたARRIVEガイドラインは、動物実験計画において最低限記載すべき項目をまとめたものであり、Natureをはじめ多くの学術雑誌に支持されているガイドラインです。
そもそもこのガイドラインが作成された背景には、動物実験の再現性があまりにも低い(一説には70%以上の実験が再現できない)と言われてきたことがあります。その一因として実験方法の詳細が述べられていないとの指摘がありました。
英国の機関が、動物実験の記載がある271報(1999-2005)の論文を精査したところ、研究の仮説・目的を記載し、かつ動物の数と特徴が記載されていたのは271報のうち、わずか59%であったことを報告(https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0007824)しています。
これらの事を受けてNC3Rsは記載すべき20の項目を定めて2010年にARRIVEガイドラインとして発表しました。多くの研究機関や出版社から支持されてきたものの、記載項目が多いことからも問題の根本的な解決には至りませんでした。そこで改訂版であるARRIVEガイドライン2.0が新たに公開されました。
ARRIVEガイドライン2.0の主な変更点は以下のとおりです。
記載すべき最低限の項目を10項目に絞った「ARRIVE Essential 10」とそれらを補完する「Recommended Set」に分類した
ARRIVE Essential 10は以下のとおりです。なお正式な日本語訳は日本実験動物学会等、公的機関によるアナウンスをお待ちください。
1. Study design(研究計画)
2. Sample size(サンプルサイズ)
3. Inclusion and exclusion criteria(包含基準と除外基準)
4. Randomisation(ランダム化)
5. Blinding(盲検化)
6. Outcome measures(実験の帰結)
7. Statistical methods(統計学的方法)
8. Experimental animals(実験動物の情報)
9. Experimental procedures(実験処置)
10. Results(結果)
前回のガイドラインが20項目であったことからも項目数を絞って記載しやすくなっていることが分かります。通常の動物実験審査においては3~5の項目を審査することは少ないのですが、今後はこのあたりも審査することが求められてくるかもしれません。














