文献紹介:SDラットにおけるアルファキサロン及びアルファキサロン-デクスメデトミジン混合麻酔の腹腔内投与

Intraperitoneal Alfaxalone and Alfaxalone–Dexmedetomidine Anesthesia in Sprague–Dawley Rats (Rattus norvegicus)
Authors: West, Sylvia E; Lee, Jonathan C; Johns, Tinika N; Nunamaker, Elizabeth A
Source: Journal of the American Association for Laboratory Animal Science
Publisher: American Association for Laboratory Animal Science
DOI: https://doi.org/10.30802/AALAS-JAALAS-19-000161
Appeared or available online: 2020/08/05
【概要】
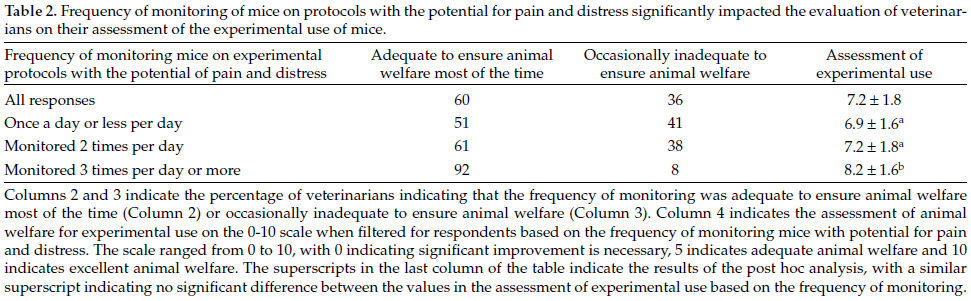
予測不可能性や効果の変化があるため、実験用げっ歯類における注射麻酔薬のレジメンは洗練されたものとなっている。本研究では,近年獣医学的に人気が高まっているアルファキサロンを単独およびデクスメデトミジンと併用して,SDラットに腹腔内投与した場合の麻酔能を評価することを試みた。アルファキサロンのみの3用量と、アルファキサロン-デクスメデトミジンの4用量の組み合わせを雄ラットと雌ラットで試験した。誘導までの時間、麻酔時間、脈拍数、呼吸数、体温、回復までの時間を盲検化された観察者によって記録した。様々な麻酔プロトコルによって誘導された麻酔のレベルは、有害な刺激に対するペダル離脱反射を用いて評価し、反応に応じてスコア化した。処置群に依存して、アティパメゾールまたは生理食塩水を、動物が麻酔の60分に達した時点で腹腔内投与した。投与量にかかわらず、アルファキサロン単独では鎮静レベルの麻酔しか達成できなかったのに対し、アルファキサロン-デクスメデトミジンの組み合わせはすべての動物において外科レベルの麻酔をもたらした。アルファキサロン単独およびデクスメデトミジンとの併用による麻酔レジメンは性差を示し、雌ラットは雄ラットよりも長時間の鎮静または麻酔を維持した。雌雄ともに、デクスメデトミジンの効果と一致する生理的パラメータの減少を示した。以上の結果から、雌ラットの手術麻酔には、鎮静には20mg/kgのアルファキサロンを、手術麻酔には30mg/kgのアルファキサロンと0.05mg/kgのデクスメデトミジンを併用することを推奨する。雄性ラットに対するアルファキサロンのみおよびアルファキサロン-デクスメデトミジンの適切な用量は、本研究では決定されておらず、さらなる評価が必要である。
注射用麻酔でどこまで外科手術をするかという事がありますが、現在、実験動物で多く使用されている三種混合麻酔(メデトミジン、ミダゾラム、ブトルファノール)は血糖値の上昇や体温の低下などの副作用があり若干使いづらい印象があるので、代替麻酔の開発には大いに賛成。でも今回の結果はかなり性差があることが示唆されているため、その点についてはフォローが必要かなという印象です。
ちなみに代替麻酔の話で、日本国内では2020年8月7日にムンディファーマが超短時間作用型の静脈麻酔薬アネレム(一般名:レミマゾラムベシル酸塩)を発売しました。レミマゾラムは日経メディカルの記事にこういった記載があります。
レミマゾラムは、既存のミダゾラムと同じベンゾジアゼピン系全身麻酔薬である。循環抑制作用が少なく、投与時の注射部位反応が少ないこと、拮抗薬フルマゼニルによって拮抗されることなど、既存のミダゾラムと同様の利点もある。ミダゾラムと類似した構造を有しているが、レミマゾラムはジアゼピン環にエステル結合の側鎖を持ち、主に肝臓の組織エステラーゼによって速かに代謝される超短時間作用型静注製剤となっている。また、代謝に肝薬物代謝酵素CYPが関与しておらず、代謝物に活性がないことも、ミダゾラムとの大きな相違点となっている。レミマゾラムはこうした特徴から、高齢者や循環動態が不安定な患者を含め、全身麻酔を施行する幅広い患者に対して有効かつ安全性の高い薬剤として期待されている。
2020/03/13 北村 正樹(東京慈恵会医科⼤学附属病院薬剤部)CYPを介さず代謝される超短時間作用型ベンゾジアゼピン系全身麻酔薬
https://medical.nikkeibp.co.jp/leaf/all/series/drug/update/202003/564675.html
代謝にCYPが関与していないのは良いですね。ミダゾラムは3A4によって代謝されるため併用注意が結構ありましたし。加えて、日本人の全身麻酔施行手術患者を対象とした国内第2/3相実薬対照無作為化単盲検比較試験(対照薬:プロポフォール)において、プロポフォールに対する本薬の非劣性が検証されたとの記載もありますので、むしろプロポの代替麻酔として臨床の方が使用されるのも良いのかもしれませんね。
(本コラムの引用文献、図は、クリエイティブコモンズライセンスの下に提供されています。)
関連記事
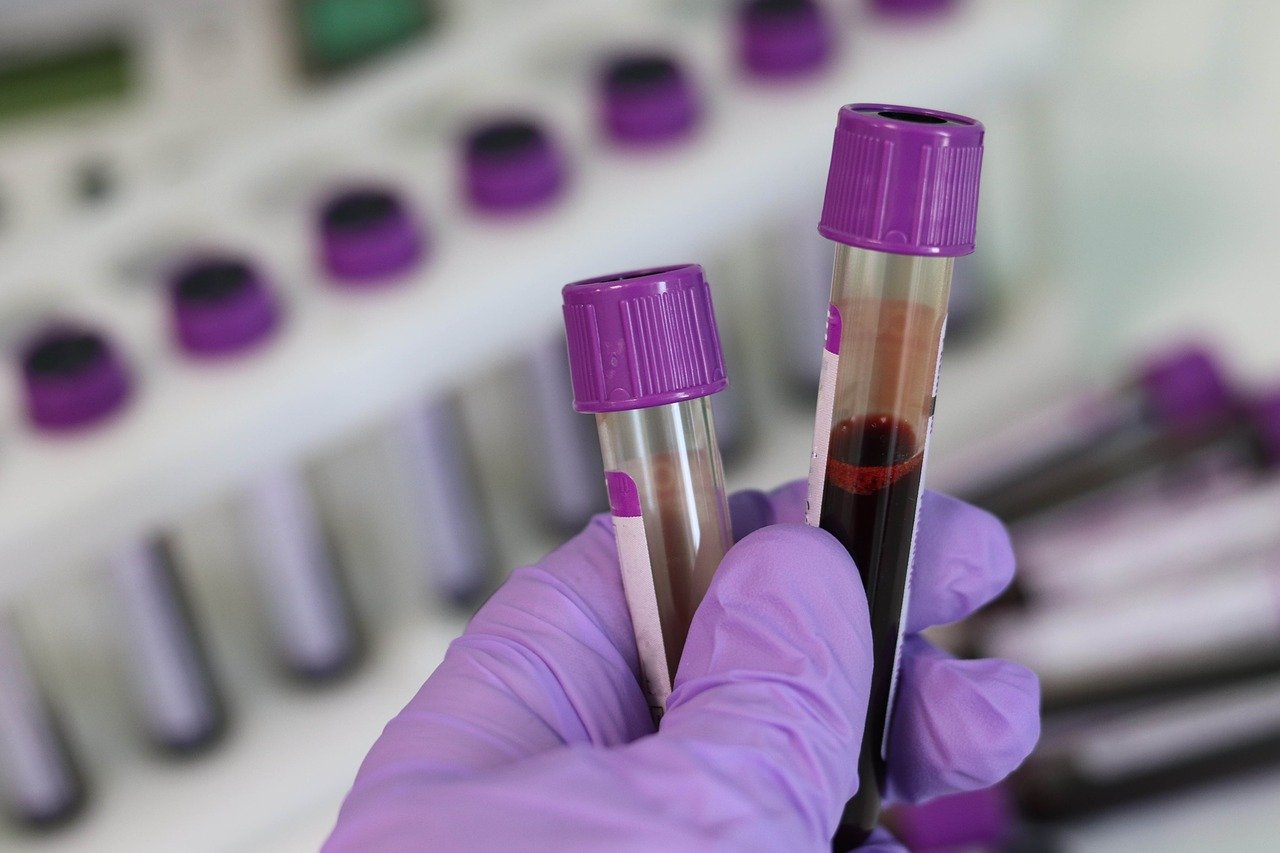
実験動物の微生物検査
実験動物は一般に販売されている動物と異なり、特定の病原体を有していないことが明らかになっているSPF(Specific Pathogen Free)動物が多く用いられています。これは病原体が動物に与える影響(ノイズ)を排除するためなのですが、では一般の動物はどの程度、病原体に汚染されているのでしょうか。2015年に日本国内のペットショップで販売されているマウスの病原体保有状況を調べた報告(Hayashimoto N et al. Exp Anim. 2015;64:155-160.)がありますが、そちらの報告によると神奈川県と東京都の5つのペットショップに由来する28匹のマウスを検査したところ、以下のような結果(検出率)が得られたとのことです。
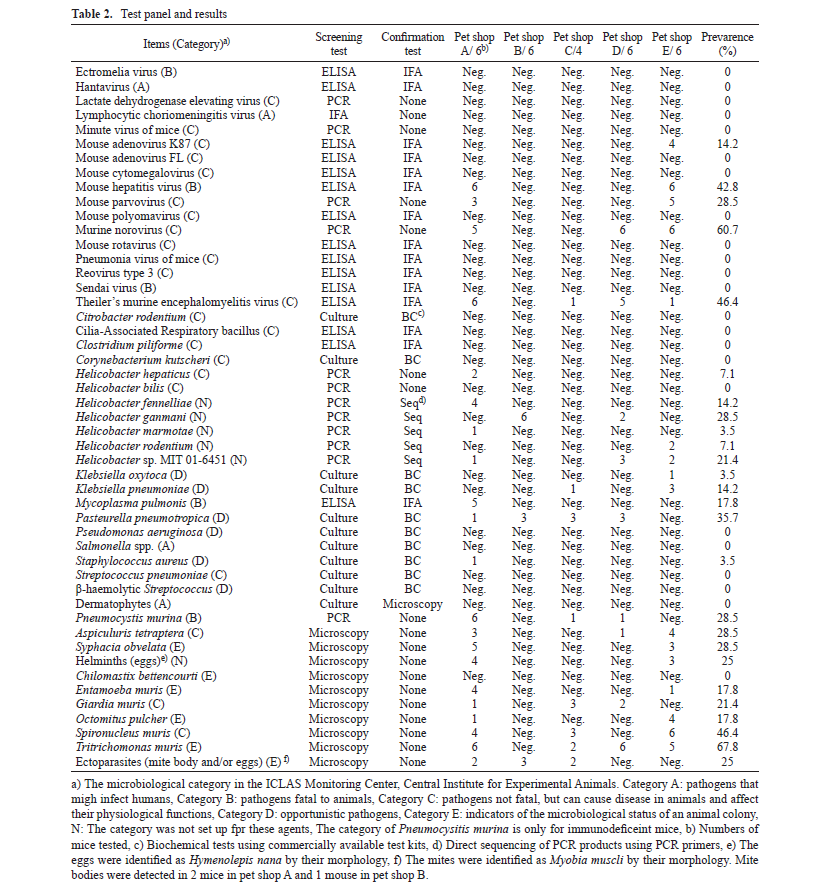
このようにペットショップごとにその検出率は異なるものの、多くの動物が微生物汚染を受けていることが分かりました。なお、人獣共通感染症を引き起こす病原体は検出されませんでしたが、動物に影響を及ぼす病原体は複数のペットショップから検出されています。これらの病原体は一般に飼育されている状態では特に問題がないことも多いのですが、動物実験に用いる際には状況が変わってきます。冒頭でも述べましたが、実験動物は余計なノイズを排除する必要があります。「再現性」は動物実験において最も重要な一つの要素ですが、動物によって病原体を持っていたり持っていなかったりすると、動物の状態が安定せず、試験結果の信頼性に影響する場合があります。また、このことによって実験に用いる動物の数が多くなってしまうことは避けるべきです。

ARRIVEガイドライン2.0が公開されました
7月14日にNC3Rs(英国3Rセンター)にてARRIVEガイドライン2.0が公開(https://arriveguidelines.org/)されました。2010年に初めて公開されたARRIVEガイドラインは、動物実験計画において最低限記載すべき項目をまとめたものであり、Natureをはじめ多くの学術雑誌に支持されているガイドラインです。
そもそもこのガイドラインが作成された背景には、動物実験の再現性があまりにも低い(一説には70%以上の実験が再現できない)と言われてきたことがあります。その一因として実験方法の詳細が述べられていないとの指摘がありました。
英国の機関が、動物実験の記載がある271報(1999-2005)の論文を精査したところ、研究の仮説・目的を記載し、かつ動物の数と特徴が記載されていたのは271報のうち、わずか59%であったことを報告(https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0007824)しています。
これらの事を受けてNC3Rsは記載すべき20の項目を定めて2010年にARRIVEガイドラインとして発表しました。多くの研究機関や出版社から支持されてきたものの、記載項目が多いことからも問題の根本的な解決には至りませんでした。そこで改訂版であるARRIVEガイドライン2.0が新たに公開されました。
ARRIVEガイドライン2.0の主な変更点は以下のとおりです。
記載すべき最低限の項目を10項目に絞った「ARRIVE Essential 10」とそれらを補完する「Recommended Set」に分類した
ARRIVE Essential 10は以下のとおりです。なお正式な日本語訳は日本実験動物学会等、公的機関によるアナウンスをお待ちください。
1. Study design(研究計画)
2. Sample size(サンプルサイズ)
3. Inclusion and exclusion criteria(包含基準と除外基準)
4. Randomisation(ランダム化)
5. Blinding(盲検化)
6. Outcome measures(実験の帰結)
7. Statistical methods(統計学的方法)
8. Experimental animals(実験動物の情報)
9. Experimental procedures(実験処置)
10. Results(結果)
前回のガイドラインが20項目であったことからも項目数を絞って記載しやすくなっていることが分かります。通常の動物実験審査においては3~5の項目を審査することは少ないのですが、今後はこのあたりも審査することが求められてくるかもしれません。

 JALAM学術集会委員会
JALAM学術集会委員会