実験動物のための水分補給・栄養補給用ジェル
コラム 動物実験

通常の動物実験では、マウス・ラットなどの小動物は自由にエサや水を摂取することが出来るようになっています。

https://www.sciencenews.org/article/sex-differences-bias-male-female-lab-animals
しかし疾患モデルだったり、手術後の回復期などでは立ち上がってエサや水を摂取することが難しい場合があります。そのような場合には動物福祉の観点から水分補給・栄養補給を目的としたジェルをケージの中に置くことがあり、その際に良く利用される市販品がClearH2O社(https://www.clearh2o.com/)のHydroGelなどです。

個人的にも実験の際に使用していましたが、滅菌された状態で個別になっているので、蓋のシールを剥がしてやってケージの中に入れれば済むといったお手軽さが非常に良かった印象です。また、動物の状態によっても様々なタイプのジェルを使い分けることが出来ます。
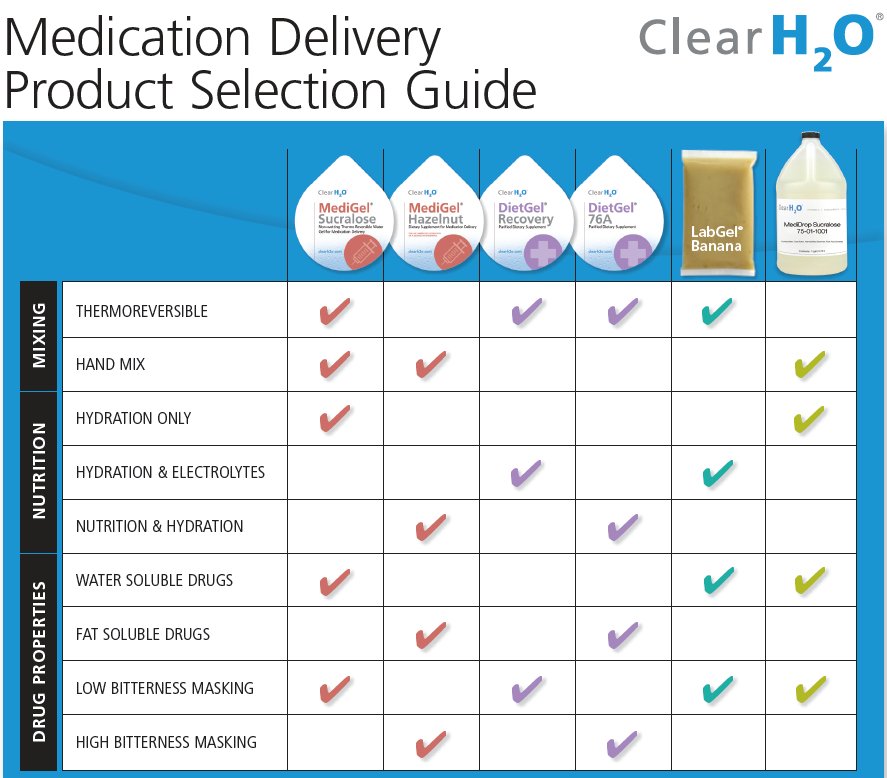
水分補給のみだったらHydrogel、術後の回復には電解質バランスを整えるためのDietgelのRecovery、立ち上がるのが難しいような疾患モデルにはエサと水の要素を兼ね備えたDietgelの76Aといった感じで使い分けていました。HPを見るとサルなどの大動物にも薬の苦みなどをマスキングして使えるようですね。
以前は術後鎮痛のために鎮痛剤(カルプロフェン)が含まれていたジェルもあったのですが、FDA(アメリカ食品医薬品局)が厳しくなったとかで製造が中止になってしまいました。手術直後にオピオイドを打って、あとは鎮痛剤入りのジェルで2~3日様子見が出来ただけに無くなってしまったことが悔やまれます。とはいえ今販売されているジェルにも薬を混ぜ込んで投与できるとのことですので、事前準備に十分な時間がかけられる場合には試してみるのも良さそうです。
また、消費期限は常温で製造日から24カ月とのことですので、災害などで断水が起きた際の緊急用としてストックしておくのも良いと思います。実際、とある製薬会社では東日本大震災で研究所が被災し、断水になった際にこちらのジェルで動物を維持したと伺っています。このように動物福祉の観点からだけではなく、防災に備えるためのBCPの一環としても、いつでも使用できるように備えておくのが望ましいと考えています。
関連記事
実験動物の微生物検査
実験動物は一般に販売されている動物と異なり、特定の病原体を有していないことが明らかになっているSPF(Specific Pathogen Free)動物が多く用いられています。これは病原体が動物に与える影響(ノイズ)を排除するためなのですが、では一般の動物はどの程度、病原体に汚染されているのでしょうか。2015年に日本国内のペットショップで販売されているマウスの病原体保有状況を調べた報告(Hayashimoto N et al. Exp Anim. 2015;64:155-160.)がありますが、そちらの報告によると神奈川県と東京都の5つのペットショップに由来する28匹のマウスを検査したところ、以下のような結果(検出率)が得られたとのことです。
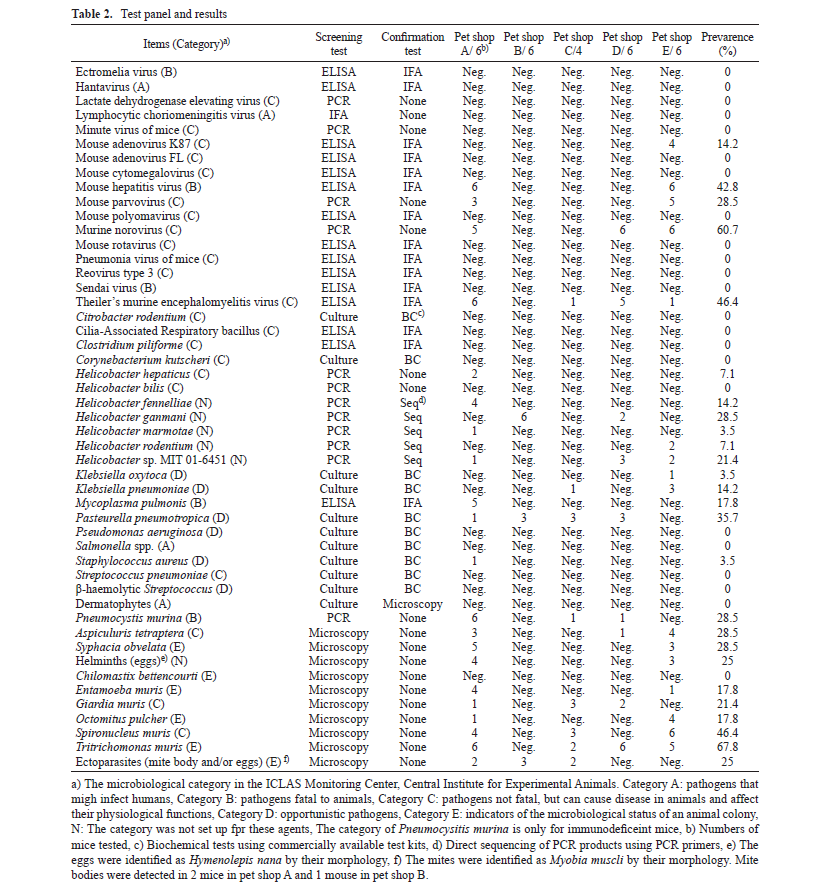
このようにペットショップごとにその検出率は異なるものの、多くの動物が微生物汚染を受けていることが分かりました。なお、人獣共通感染症を引き起こす病原体は検出されませんでしたが、動物に影響を及ぼす病原体は複数のペットショップから検出されています。これらの病原体は一般に飼育されている状態では特に問題がないことも多いのですが、動物実験に用いる際には状況が変わってきます。冒頭でも述べましたが、実験動物は余計なノイズを排除する必要があります。「再現性」は動物実験において最も重要な一つの要素ですが、動物によって病原体を持っていたり持っていなかったりすると、動物の状態が安定せず、試験結果の信頼性に影響する場合があります。また、このことによって実験に用いる動物の数が多くなってしまうことは避けるべきです。

ARRIVEガイドライン2.0が公開されました
7月14日にNC3Rs(英国3Rセンター)にてARRIVEガイドライン2.0が公開(https://arriveguidelines.org/)されました。2010年に初めて公開されたARRIVEガイドラインは、動物実験計画において最低限記載すべき項目をまとめたものであり、Natureをはじめ多くの学術雑誌に支持されているガイドラインです。
そもそもこのガイドラインが作成された背景には、動物実験の再現性があまりにも低い(一説には70%以上の実験が再現できない)と言われてきたことがあります。その一因として実験方法の詳細が述べられていないとの指摘がありました。
英国の機関が、動物実験の記載がある271報(1999-2005)の論文を精査したところ、研究の仮説・目的を記載し、かつ動物の数と特徴が記載されていたのは271報のうち、わずか59%であったことを報告(https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0007824)しています。
これらの事を受けてNC3Rsは記載すべき20の項目を定めて2010年にARRIVEガイドラインとして発表しました。多くの研究機関や出版社から支持されてきたものの、記載項目が多いことからも問題の根本的な解決には至りませんでした。そこで改訂版であるARRIVEガイドライン2.0が新たに公開されました。
ARRIVEガイドライン2.0の主な変更点は以下のとおりです。
記載すべき最低限の項目を10項目に絞った「ARRIVE Essential 10」とそれらを補完する「Recommended Set」に分類した
ARRIVE Essential 10は以下のとおりです。なお正式な日本語訳は日本実験動物学会等、公的機関によるアナウンスをお待ちください。
1. Study design(研究計画)
2. Sample size(サンプルサイズ)
3. Inclusion and exclusion criteria(包含基準と除外基準)
4. Randomisation(ランダム化)
5. Blinding(盲検化)
6. Outcome measures(実験の帰結)
7. Statistical methods(統計学的方法)
8. Experimental animals(実験動物の情報)
9. Experimental procedures(実験処置)
10. Results(結果)
前回のガイドラインが20項目であったことからも項目数を絞って記載しやすくなっていることが分かります。通常の動物実験審査においては3~5の項目を審査することは少ないのですが、今後はこのあたりも審査することが求められてくるかもしれません。

 JALAM学術集会委員会
JALAM学術集会委員会