実験動物の安楽死方法

愛玩動物や展示動物などの終生飼育動物とは違い、実験動物は非終生飼育動物であるため、基本的には安楽死によってその生涯を終えます(里親制度除く)。動物実験従事者が守るべきガイドラインのひとつでもある、環境省の「実験動物の飼養及び保管並びに苦痛の軽減に関する基準」には安楽死に関する以下の記載があります。
実験動物管理者、実験実施者及び飼養者は、実験等を終了し、若しくは中断した実験動物又は疾病等により回復の見込みのない障害を受けた実験動物を殺処分する場合にあっては、速やかに致死量以上の麻酔薬の投与、頸(けい)椎(つい)脱臼(きゅう)等の化学的又は物理的方法による等指針に基づき行うこと。
この事を受け、各施設では独自に安楽死に対する規程を作成し実施していると思いますが、それらの規範となるものがAVMA(米国獣医学会)の安楽死に関するガイドライン(https://www.avma.org/resources-tools/avma-policies/avma-guidelines-euthanasia-animals)です。
こちらのガイドラインは実験動物に限ったものではなく、愛玩動物や産業動物など様々な分野の動物に対する安楽死方法が科学的視点から規定されています。安楽死に関しては動物が苦しむことなく死を迎える必要があり、それにはどうしても科学的根拠が必要になるため、このガイドラインは国内の各施設でも非常に重宝されています。また本ガイドラインは2020年に更新された非常に新しいものです(7年ぶりに更新)。
動物実験関係者だけでなく、動物に関わる全ての方に見て頂きたいガイドラインなのですが、いかんせん英語で全121ページという膨大な量のため足踏みしてしまう方が多いと思います。その時に参考になるのがミシガン大学のガイドライン(https://az.research.umich.edu/animalcare/guidelines/university-michigan-euthanasia-guidelines)です。
こちらはAVMAガイドラインとは異なり、イヌでCO2での安楽死が不可になっているなど若干の改変はありますが、実験動物としては現場に即したものであり、なおかつペントバルビタールなどのバルビツールによる静脈内麻酔など優先度の高い化学的安楽死方法が上に来ていることも動物に対する苦痛度を考えた上で非常に使いやすいものとなっています。
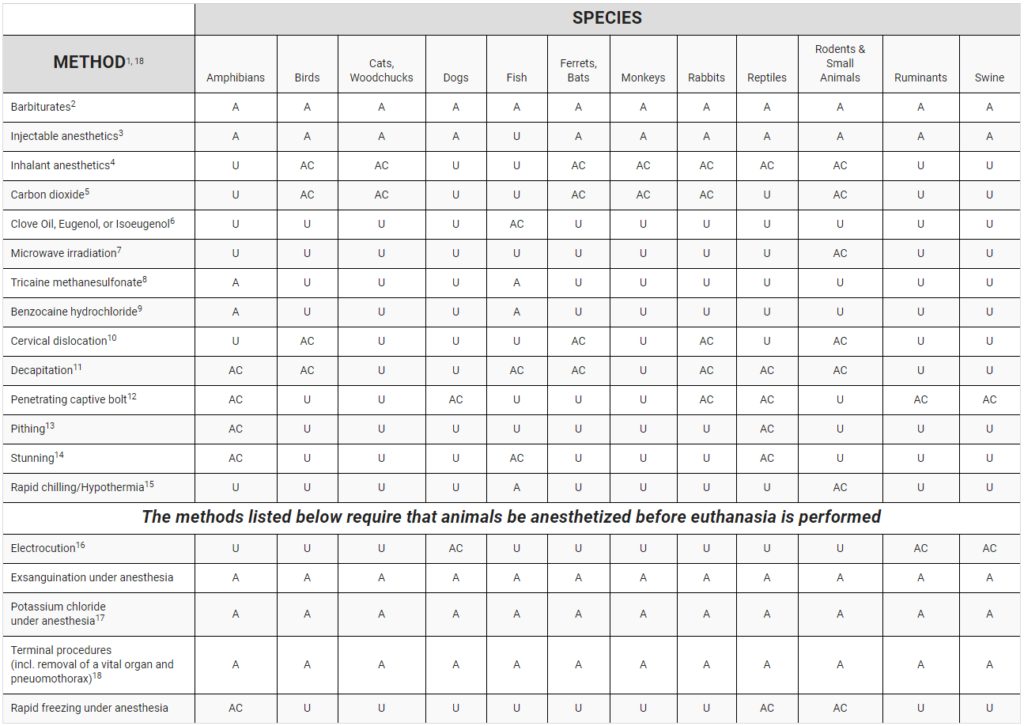
なお、表の読み方は以下のとおりです。
A = Acceptable – those which consistently produce a humane death when used as the sole means of euthanasia
AC = Acceptable with Conditions – those which consistently produce a humane death when specific conditions are met
U = Unacceptable – deemed inhumane under any conditions, or found to pose substantial risk to human applying the technique
そしてここからは非公式になりますが、私の方で勝手にこのミシガン大学の安楽死ガイドラインの表を翻訳してみました。
-1024x657.png)
安楽死に関する情報は日進月歩の状態です。前回2013年の時にはCO2での安楽死は10~30%/minでの流速で容器内の空気を置換していくと良いとされていたのですが、今回の改訂では30~70%/minで置換していく方が実は動物にとって負担が少なかったとの報告がなされています。また、魚類の安楽死も現在は化学物質による安楽死法がメインですが、2019年にヨーロッパで開催された学会では低体温での安楽死の方が苦痛が少ないことが示唆されたとの報告もされています。このように安楽死といった最後にできる実験処置としては、動物の苦痛の軽減を何よりも優先して、情報をアップデートしていく必要があると考えています。
関連記事
実験動物の微生物検査
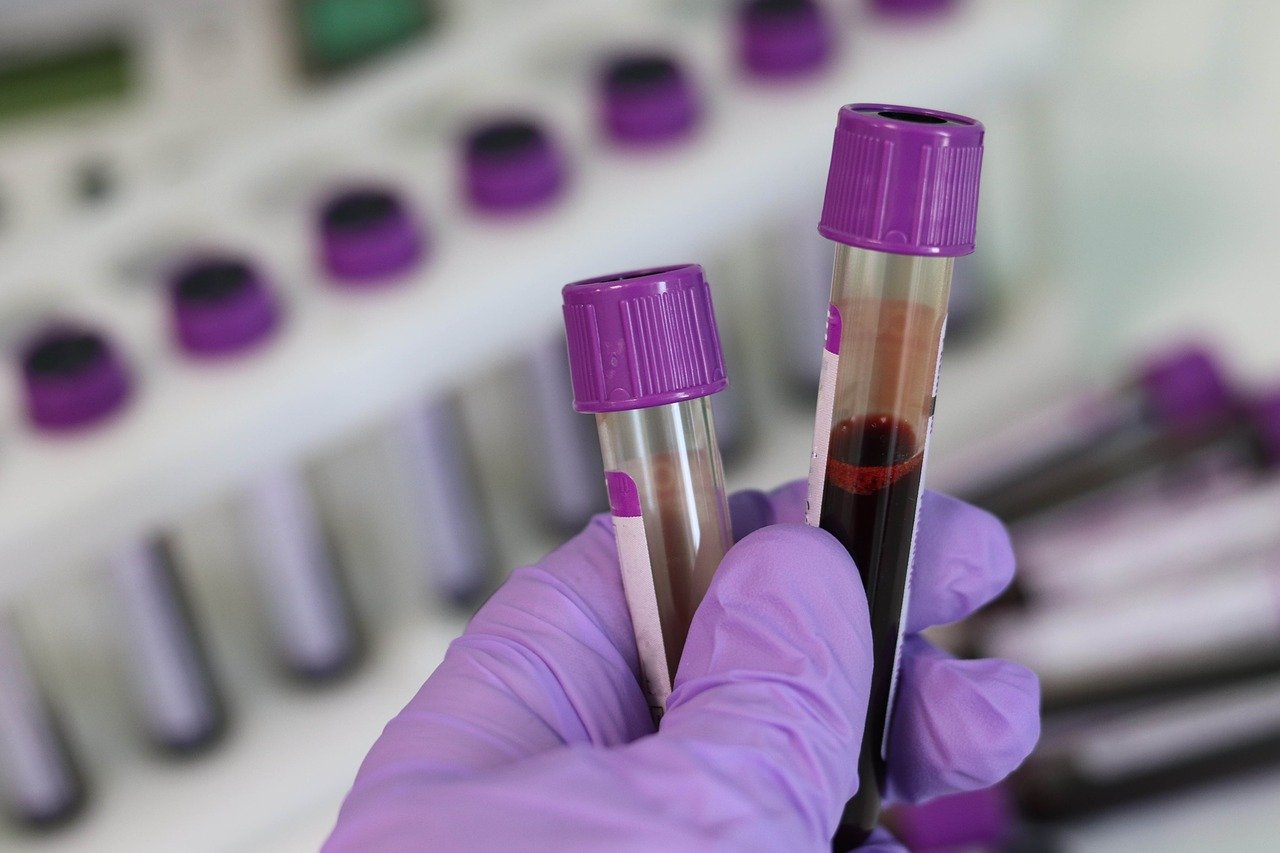
実験動物は一般に販売されている動物と異なり、特定の病原体を有していないことが明らかになっているSPF(Specific Pathogen Free)動物が多く用いられています。これは病原体が動物に与える影響(ノイズ)を排除するためなのですが、では一般の動物はどの程度、病原体に汚染されているのでしょうか。2015年に日本国内のペットショップで販売されているマウスの病原体保有状況を調べた報告(Hayashimoto N et al. Exp Anim. 2015;64:155-160.)がありますが、そちらの報告によると神奈川県と東京都の5つのペットショップに由来する28匹のマウスを検査したところ、以下のような結果(検出率)が得られたとのことです。
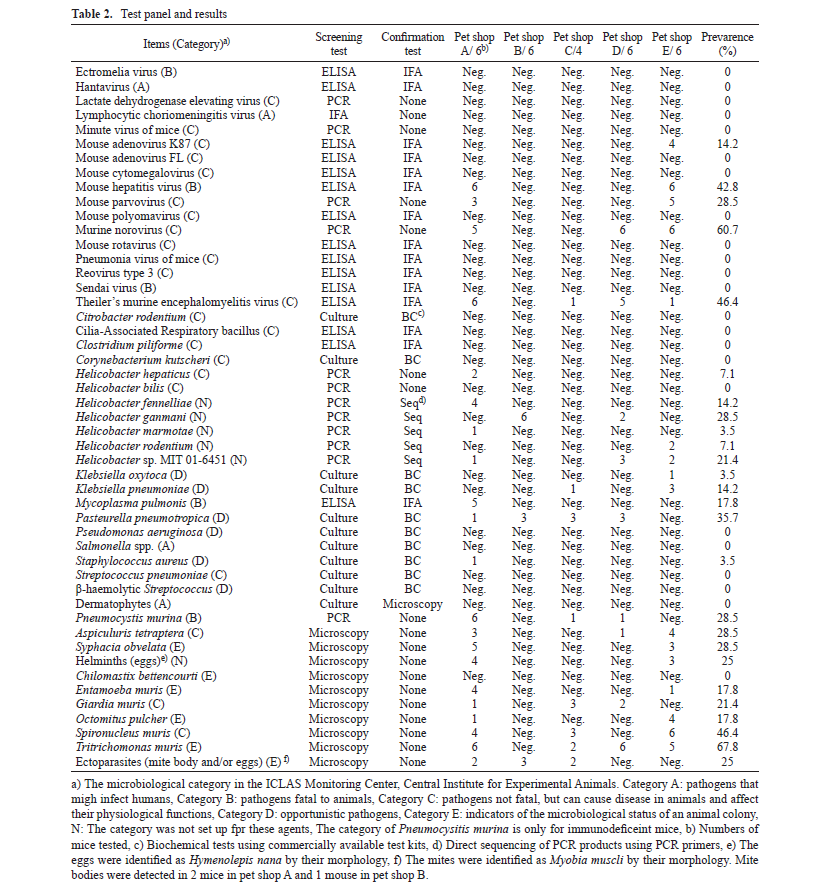
このようにペットショップごとにその検出率は異なるものの、多くの動物が微生物汚染を受けていることが分かりました。なお、人獣共通感染症を引き起こす病原体は検出されませんでしたが、動物に影響を及ぼす病原体は複数のペットショップから検出されています。これらの病原体は一般に飼育されている状態では特に問題がないことも多いのですが、動物実験に用いる際には状況が変わってきます。冒頭でも述べましたが、実験動物は余計なノイズを排除する必要があります。「再現性」は動物実験において最も重要な一つの要素ですが、動物によって病原体を持っていたり持っていなかったりすると、動物の状態が安定せず、試験結果の信頼性に影響する場合があります。また、このことによって実験に用いる動物の数が多くなってしまうことは避けるべきです。

ARRIVEガイドライン2.0が公開されました
7月14日にNC3Rs(英国3Rセンター)にてARRIVEガイドライン2.0が公開(https://arriveguidelines.org/)されました。2010年に初めて公開されたARRIVEガイドラインは、動物実験計画において最低限記載すべき項目をまとめたものであり、Natureをはじめ多くの学術雑誌に支持されているガイドラインです。
そもそもこのガイドラインが作成された背景には、動物実験の再現性があまりにも低い(一説には70%以上の実験が再現できない)と言われてきたことがあります。その一因として実験方法の詳細が述べられていないとの指摘がありました。
英国の機関が、動物実験の記載がある271報(1999-2005)の論文を精査したところ、研究の仮説・目的を記載し、かつ動物の数と特徴が記載されていたのは271報のうち、わずか59%であったことを報告(https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0007824)しています。
これらの事を受けてNC3Rsは記載すべき20の項目を定めて2010年にARRIVEガイドラインとして発表しました。多くの研究機関や出版社から支持されてきたものの、記載項目が多いことからも問題の根本的な解決には至りませんでした。そこで改訂版であるARRIVEガイドライン2.0が新たに公開されました。
ARRIVEガイドライン2.0の主な変更点は以下のとおりです。
記載すべき最低限の項目を10項目に絞った「ARRIVE Essential 10」とそれらを補完する「Recommended Set」に分類した
ARRIVE Essential 10は以下のとおりです。なお正式な日本語訳は日本実験動物学会等、公的機関によるアナウンスをお待ちください。
1. Study design(研究計画)
2. Sample size(サンプルサイズ)
3. Inclusion and exclusion criteria(包含基準と除外基準)
4. Randomisation(ランダム化)
5. Blinding(盲検化)
6. Outcome measures(実験の帰結)
7. Statistical methods(統計学的方法)
8. Experimental animals(実験動物の情報)
9. Experimental procedures(実験処置)
10. Results(結果)
前回のガイドラインが20項目であったことからも項目数を絞って記載しやすくなっていることが分かります。通常の動物実験審査においては3~5の項目を審査することは少ないのですが、今後はこのあたりも審査することが求められてくるかもしれません。

 JALAM学術集会委員会
JALAM学術集会委員会