- トップ
- コラム一覧
教育委員会の記事一覧

実験動物の飼育環境
東京大学大学院農学生命科学研究科獣医学専攻 准教授 角田 茂
1. とても綺麗な環境で飼育されている実験動物
コロナ禍が始まって以来、マスク、手洗いが欠かせない生活になってから、あらゆる感染症が減っていますよね。人間は普段、いかに感染性微生物にさらされて生きているのか痛感する今日この頃です。
さて、みなさんは実験動物業界の専門用語である“SPF”という言葉、ご存知ですか。
スーパーやレストランで、SPFブタ肉など、目にしたことがあるかもしれません。
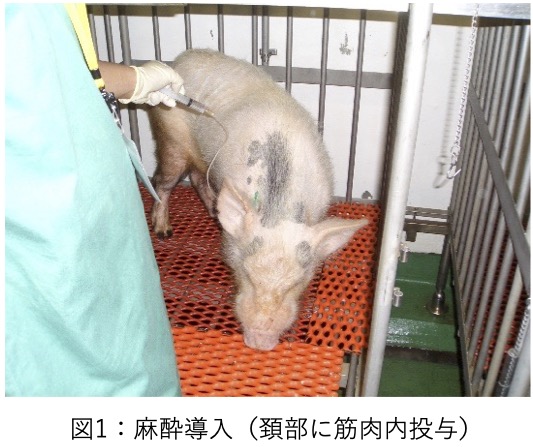
“SPF”とは「Specific Pathogen Free」の略語であり、”特定の病原性微生物を持たないことが保証されている”ということで、言うなれば微生物学的にきれい、あるいは安全であるということになります。ヒトに感染する病原体を排除して飼育すれば、抗生物質やワクチンの投与が不要になり、健康な動物を飼育することができます。1990年頃に日本に初めてSPFブタの飼育技術を導入したのは、本学会の発起人である波岡茂郎先生(1929-2014, 北大名誉教授)で、企業との共同で日本初のSPFブタを開発されました。当時、貴重な第一号のSPFブタの焼肉を、現在の本学会・会長である佐々木先生ら学生にふるまったようです。
さて、医学系の動物実験施設では、基本的にはSPF状態を保つための環境で動物が飼育されています。このSPF環境を維持するためには、バリア施設が必要であり、動物室内を陽圧に保つことにより外からの病原体の侵入をブロックするような特殊な構造の建物に、実験従事者および動物の厳密な入退室管理、滅菌・消毒した飼料や水、ケージの供給・使用など、大変なコストと労力を掛けて管理運営が行われています。
ちなみに、SPF環境維持が適切に行われていることを保証するために、定期的な微生物モニタリングが実施されています。例えば、実験動物中央研究所ICLASモニタリングセンターに検査をお願いした場合、12〜19項目のSPF対象微生物検査セットで14,500〜25,000円/匹となっていることからも、SPF維持が高コストであることがおわかりいただけるかと思います。
では、なぜ研究にSPF環境で飼育したクリーン動物を用いるのでしょうか。

マウスバイオリソースの源流 ~ラスロップ、リトルそしてジャクソン研究所
本ホームページに「マウスの系統間、亜系統間にみられる遺伝子型、表現型の違い〜C57BL/6JとC57BL/6Nとの比較を中心に」というコラムが登載されています。その中に、「C57BL/6は、C. C. リトルがA. E. ラスロップから1921年に入手したマウスから樹立したC57BL系統に由来します。C57BL/6系統は、1948年にアメリカのジャクソン研究所に導入され維持されてきました」という記載があります。リトルとジャクソン研究所については、実験動物に関わっている方や実験動物学の講義を受講した経験のある方なら一度は耳にしたことがあると思いますが、ラスロップについてはあまり馴染みの無い読者がいるかも知れません。今回は、ラスロップとリトル、リトルとジャクソン研究所の関係についてお話させていただきます。