- トップ
- コラム一覧

研究者が実践するサイエンスコミュニケーション(後編)
他の人の意見を聞く
ピアレビューと言いますが、ある程度完成した作品を他の人に見せ、意見をもらう過程が非常に重要です。特に自分の研究に関連したことは、どの程度他の人が理解できるのか感覚が鈍っていたり、一般の認識とずれが生じていることがあります。通常、ピアとは「仲間や同僚」を意味しますが、必ずしも自分と立場の近い人を選ぶ必要はありません。逆にとても遠い立場の人にお願いする必要もなく、科学研究者であっても分野が異なれば「非専門家」であり、自分には見えない気付きをもたらしてくれるはずです。伝えたい層が明確であれば、その立場に近い人をピアとして選ぶのは情報の洗練に効果的です。
現時点の日本では、科学者が積極的にサイエンスコミュニケーション活動に参画する機会はあまりないかもしれません。一方、外部競争的資金を利用する場合など、社会への情報発信を義務付けているものもあります。また近年、クラウドファンディングによる研究資金の調達も活発化しており、科学に対する社会の関心や理解を得ることは、社会課題を解決するという大義に加え、研究費の獲得に繋がります。研究の持続的発展という観点では、子どもを含めた市民の関心が高まることで、次世代の優秀な研究者が育つことも期待できます。実際に英国では、このような多角的な視点から、科学者の多くはサイエンスコミュニケーション活動に前向きな姿勢を示しています。
科学者とサイエンスコミュニケーション
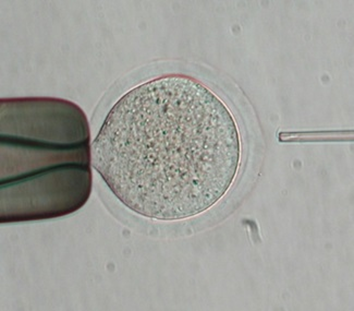
個人的な体感ですが、動物に関することは自然科学の中でも人々の関心が高く、その分、意見も多様化し、熱量も千差万別です。ただ、一般に大多数の人は動物のしあわせを願っていると私は考えています。動物実験/実験動物に関しては、世界中で常に議論がありますが、それに反対する人も科学者も、動物や人のしあわせといった、そう離れていない目標や信念を持っているのかもしれません。一方で、特定の意見こそなくても、私たちは日々、動物由来食品や製品、動物実験を経て開発された薬など、その恩恵を大いに享受して生きており、すべての人は動物に関する課題の利害関係者、ステークホルダーです。熱量の高い人だけでなく、すべてのステークホルダーがこの課題について考え、行動することが解決に必要であり、一科学者としては、サイエンスコミュニケーションを通じて多様な立場の人と情報を共有することがその一歩となると考えています。
大震災やパンデミックなど、危機的状況が発生したときのサイエンスコミュニケーションは、特にリスクコミュニケーションと呼ばれます。東日本大震災および福島第一原子力発電所事故時には、耳なじみのない専門用語が汎用されることで社会は混乱し、その重要性が強く認識されました。その反省も踏まえ、SARS-CoV-2による新型コロナウイルス感染症パンデミックでは、専門家や各学会が積極的に社会と情報を共有する動きがみられました。一方で、何が「正しい」情報なのか専門家も私たちも模索する日々を過ごし、昨日まで正しかったことが、今日から間違った情報になることを実体験しました。情報の正確性を高めるのは、真摯な科学研究による知見の蓄積しかありません。一方で、その伝え方や受け手のリテラシー、または社会的な文脈により、科学的に正しいことが社会の「正解」になるとは限らないことを、私たち研究者は意識する必要がある時代だと感じます。再生医療や人工知能など技術が高度・複雑化する一方、社会における理解と倫理的な議論が追い付いていない課題も多く、サイエンスコミュニケーションの拡がりにより、議論が活発化することを期待しています。
参考文献
1. 加納圭,水町衣里,岩崎琢哉,磯部洋明,川人よし恵,前波晴彦.サイエンスカフェ参加者のセグメンテーションとターゲティング : 「科学・技術への関与」という観点から.科学技術コミュニケーション 第13号.2013; 3-16.
コラム サイエンスコミュニケーション

研究者が実践するサイエンスコミュニケーション(前編)
サイエンスコミュニケーションにおいて、受け手からの反応はさまざまで、自分の発した言葉に対し批判的な意見が返ってくることもあり、伝え手にとっては気持ち良いものではないかもしれません。ですが、自分が投じた情報により、伝えられた側がそれを受け止め、考え、意見を持ったという点で双方向性のコミュニケーションとしては大成功です。一方、隙のない完璧な知見の提供は伝え手の満足度は高いかもしれませんが、受け手が“へーそうなんだ”や“自分には関係ないことだ”と完結してしまった場合、それは一方向性のコミュニケーションとなります。サイエンスコミュニケーションの目的は社会における課題解決であり、「分かりやすく」そして「正確に」伝えることは非常に重要な過程ですが、ゴールではありません。
もう一つの原則は「中立的」であることです。通常、サイエンスコミュニケーターは、科学者や科学技術とそれについて専門的知識を持たない人(非専門家)や社会の間に立ち、相互の理解を深め、両者のコミュニケーションを円滑にする役割を果たします。例えば科学者側が非専門家には理解しづらい用語を用いている場合は、理解しやすい言葉に置き換えたり、一方、社会からの疑問や意見が漠然としすぎている場合は、例を用いるなど、課題を明確にすることで科学者側もその意図をつかみやすくなります。この際、両者の立場を理解しつつも、どちらか一方を支持することや、批判することなく、中立的な立場を取り、コミュニケーションのバランスを取ることが求められます。自身の研究について述べるとき、中立性を維持することは難しいかもしれませんが、「受け手がどう捉えるか、または捉え得るか」を意識することは、中立性に繋がります。
ここまで、サイエンスコミュニケーションの背景や基本的な考え方をみてきました。後編では、実際にサイエンスコミュニケーションを実践するときのテクニックや課題について述べていきます。
参考文献
1. 文部科学省「サイエンスコミュニケーションとは?」(2022年8月2日閲覧)
2. 吉岡直人.地球科学におけるトランス・サイエンスの諸問題.公益財団法人深田地質研究所年報.2017.
3. 香田正人.ポスト・ノーマルサイエンスとグローバル感度解析.横幹 5 巻 1 号.2011; 37-40.
4. 荻野晴之.福島第一発電所事故後 9 か月間の放射線リスクコミュニケーションに関する省察.保健物理 47 巻 1 号.2012; 37-43.
5. 元村有希子.科学コミュニケーターのキャリア形成 ~英国の現状~.科学技術コミュニケーション 第4号.2008; 69-77.
コラム サイエンスコミュニケーション

がんも遺伝する:モード・スライの功績
彼女の楽しみは詩を書くことだった。1934年と1936年の2冊の詩集を出版し、約700編の詩を発表した。一部の詩は彼女の科学への献身的な取り組みを物語っている。
I pace the world because I am storm-driven, By this compelling of creation.
「私が世界を歩むのは、この創造の説得力によって駆り立てられているからである」
The robin does not wait to ask you like his song, He sings because he must.
「コマドリは自分の歌が好きかどうかを聞くために待つのではなく、必要だから歌うのだ」
スライの時代には、解析手法がなかったこともあり、がんの遺伝様式の観察に留まり、がんの原因や発症メカニズムを見出すことはできなかった。がんの発生機序は、がん遺伝子SRC(1976年)やRASの発見(1982年)、がん抑制遺伝子RBの発見(1986年)をきっかけに解明されていくのは周知の通りである。また、多数の遺伝子が作用し、さらに環境要因が加わって起こる病気のことを多因子疾患というが、がんの多くは、正に多因子疾患である。多因子疾患の原因遺伝子の同定が可能になるには、2000年代まで待たなければならなかった。
本コラムでは、あまり語られることはありませんが、重要な発見し、且つ心に残る研究者を取り上げました。彼女の根気よく真実に迫る執念や持続性を、是非、見習いたいものです。また、古のマウス研究者達の努力と功績に感謝しつつ、この分野の発展に微力ながら貢献したいと思いながら、筆を置かせて頂きます。
参考文献
[1] Robert Yerkes, The Dancing Mouse: A Study in Animal Behavior. 1907.
[2] https://www.jax.org/strain/000275
[3] Wilson SM et al, Mutations in Cdh23 cause nonsyndromic hearing loss in waltzer mice. Genomics. 74(2):228-233. 2001.
[4] Di Palma F et al, Mutations in Cdh23, encoding a new type of cadherin, cause stereocilia disorganization in waltzer, the mouse model for Usher syndrome type 1D. Nat Genet. 27(1):103-107. 2001.
[5] Bolz H et al, Mutation of CDH23, encoding a new member of the cadherin gene family, causes Usher syndrome type 1D. Nat Genet. 27(1):108-112. 2001.
[6] Abbie Lathrop & Leo Loeb, Further investigations on the origin of tumors in mice. V: The tumor rate in hybrid strains. Journal of Experimental Medicine. 28(4): 475-500. 1918.
[7] Ernest Tyzzer. A study of heredity in relation to the development of tumors in mice. The Journal of Medical Research. 17(2):199-211. 1907.
[8] Clarence Little & Ernest Tyzzer. Further experimental studies on the inheritance of susceptibility to a transplantable tumor, carcinoma (J.W.A.) of the Japanese waltzing mouse. The Journal of Medical Research. 33(3): 393-453. 1916.
[9] Maud Slye, The incidence and inheritability of spontaneous cancer in mice. The Journal of Medical Research 32: 159–172. 1915.
[10] https://mag.uchicago.edu/science-medicine/storm-driven
[11] https://www.lib.uchicago.edu/ead/rlg/ICU.SPCL.SLYEM.pdf Guide to the Maud Slye Papers 1910s-1930s, University of Chicago Library.
[12] Maud Slye, Proceedings. The genetics of cancer in mice. Forty-first annual meeting of the United States livestock sanitary association. 241-257. 1937

米国獣医学会(AVMA)動物の安楽死指針2020年版出版記念 -紹介動画-
日本実験動物医学専門医協会は、AVMAと翻訳契約を取り交わし、「米国獣医学会 動物の安楽死指針(安楽死ガイドライン):2020年」版の翻訳本(翻訳者代表 黒澤努、鈴木真)を出版しました。本ガイドラインは、国際的に容認される具体的な安楽死法を示しており、主に獣医師を対象に記載されています。専門的ではありますが、最新の情報を網羅しており、獣医師以外の動物にかかわる方々の指針としても重要な文献です。(原文はこちら)
2013年度版から改訂された2020年版では、第3章にS1コンパニオンアニマル、S2実験動物、S3家畜、S4馬、S5鳥類、S6魚類と水生無脊椎動物、S7野生動物と7つの動物に区分されて記載されています。
日本実験動物医学会および日本実験動物医学専門医協会は、本指針が広く周知されることで、わが国の動物福祉がより向上することを期待します。また、実験動物ならびにその他の動物の人道的な取り扱いを広めるための啓蒙活動を継続していきます。
米国獣医学会(AVMA)動物の安楽死指針(安楽死ガイドライン)2020年版の紹介
炭酸ガスを用いた安楽死
Compassion Fatigue(共感疲労)
Compassion Fatigueについて、さらに知りたい方はこちらもご覧ください。

マウスバイオリソースの源流 ~ラスロップ、リトルそしてジャクソン研究所
3. 現在のジャクソン研究所とホームページ
ジャクソン研究所(以下、JAX)のホームページ(https://www.jax.org/)には「2019年に設立90周年を迎えた」旨の記述が見られます。これは、1929年のリトルによる「ジャクソン記念研究所」設立からの年数と一致します。ホームページによると、設立当初8人だった従業員は現在では約3,000人を擁しているとのことです。現在のJAXは、リトルが最初に研究室を作ったバーハーバーのマウス研究所(ヒトの病気の遺伝的な原因を研究している)の他、同じくメイン州のエルズワース(Ellsworth)にマウスの生産所、オーガスタ(Augusta)にガン研究所、カリフォルニア州サクラメント(Sacramento)にマウスの生産所と幹細胞などの提供サービス行う研究所、コネチカット州ファーミントン(Farmington)にゲノム研究所があります。また、日本(旧・日本チャールス・リバー)や中国(上海と北京)には子会社を持ち、実験動物の生産や微生物モニタリングサービスなど実験動物に関連したサービスを提供しています。このように、リトルがマウスの研究所としてスタートさせたジャクソン記念研究所は、現在ではC57BL/6Jを初め12,000以上の実験動物の系統を維持・生産するまでに成長しています(JAXのホームページより)。しかし、大きな組織となった現在でも米国JAXはあくまで非営利のバイオメディカルの研究機関であり、マウスの供給(バイオリソース)およびマウスを通じてのヒトのゲノミクス研究のデータリソースとしての立ち位置を保っています。米国JAXは世界初のバイオリソースセンターのモデルになったわけで、まさに「ラスロップ〜リトル〜ジャクソン研究所」という流れは、「マウスバイオリソースの源流」と言えるでしょう。

今後のイベント、ウェビナー
◆:ハイブリッド開催
2022年1月
第4回 BMSA 公開セミナー ◆沖縄科学技術大学院大学(恩納村) 1月18日
日本実験動物技術者協会 関東支部 中動物部会 第35回講演会 オンライン 1月22日
2022年2月
Laboratory Animal Sciences 2022 (labroots) オンライン 2月10日
日本実験動物技術者協会 関東支部 第47回懇話会 川崎市産業振興会館(川崎市) 2月26日
2022年3月
第95回日本薬理学会年会 福岡国際会議場・福岡サンパレス(福岡市) 3月7日~9日
Meeting the Requirements of the Animal Welfare Act オンライン 3月9日、11日
第28回ヒトと動物の関係学会 学術大会 ◆慶應義塾大学日吉キャンパス(横浜市) 3月12~13日
第99回日本生理学会大会 ◆東北大学川内北キャンパス(仙台市) 3月16日~18日
日本薬学会第142年会 名古屋国際会議場(名古屋市) 3月25日~28日
2022年5月
第69回日本実験動物学会総会 仙台国際センター(仙台市) 5月18~20日
2022年6月
日本ゲノム編集学会第7回大会 オンライン 6月6日~8日
15th FELASA congress: Communication in Animal Research マルセイユ 6月13日~16日
第49回日本毒性学会学術年会 札幌コンベンションセンター(札幌市) 6月30日~7月2日