酪農学園大学獣医学類 疾患モデル学 教授 北村 浩
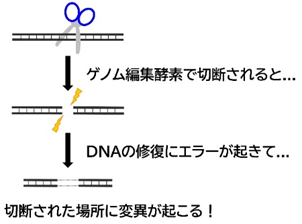
肝臓に中性脂肪が蓄積した状態を脂肪肝と呼びます。アルコールの多量な摂取により脂肪肝が生じることは古くから知られていますが、飲酒歴がない人やほとんど飲酒しない人も脂肪肝を生じることがあります。このようにアルコールを除くいろいろな原因で起こる脂肪肝の総称を非アルコール性脂肪性肝疾患(non-alcoholic fatty liver disease, NAFLD)といいます。NAFLDは肥満やメタボリックシンドロームが関与する一種の生活習慣病であり、2型糖尿病を併発することが多い疾患です。先進国における肝障害の中では最も頻度が高く、世界で4人に一人はNAFLDに罹患しているという報告もあります[17]。近年、“エネルギー代謝異常が引き起こす肝疾患”という視点に立ち、NAFLDに代わる、MAFLD(metabolic-associated fatty liver disease)という呼び方も一般的になってきています[10]。NAFLDには、比較的軽症な非アルコール性脂肪肝(non-alcoholic fatty liver, NAFL)と、炎症を伴い重症な非アルコール性脂肪性肝炎(non-alcoholic steatohepatitis, NASH)の2つの病態が知られています[15]。特にNASHは肝硬変や肝がんに進行する可能性があり、危険度の高い疾患といえます。私たち酪農学園大学獣医学類疾患モデル学ユニットでは、NAFLD克服のための新たな治療標的分子としてタンパク質の安定性を制御するユビキチン特異的プロテアーゼという酵素に注目しています。この酵素の遺伝子改変マウスがNAFLDやNASHの進行に果たす役割を調べています。このコラムではこれまで試みられたマウスの代表的なNAFLD/NASHモデルについて概説します。
1. NAFLD/NASHの典型的な病態
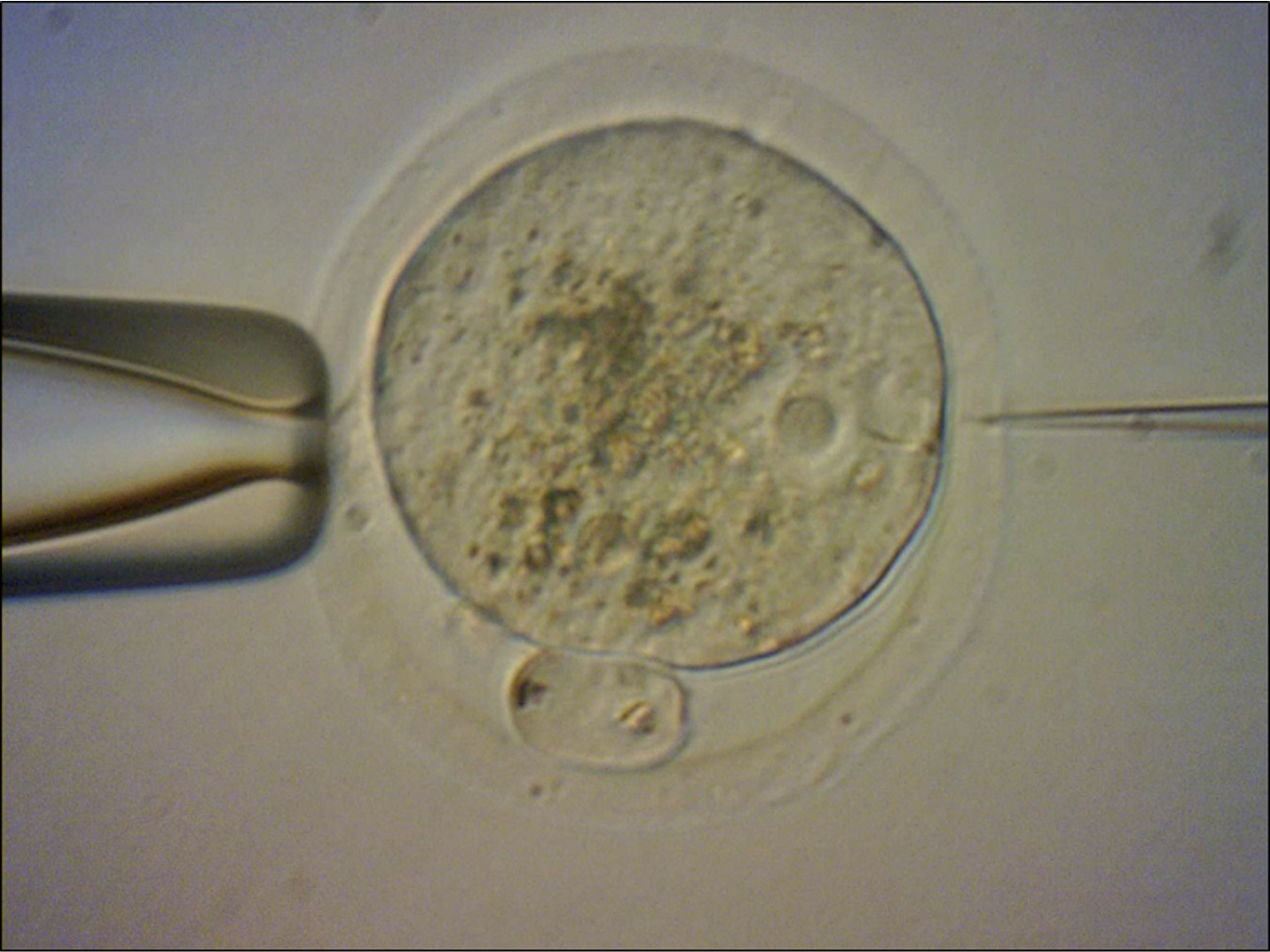
中性脂肪が肝細胞に蓄積する脂肪肝はNAFLD患者で共通にみられる病態です。NAFLの状態から更に病状が深刻なNASHへ移行するかは様々な要因により決定されます。NAFLD患者の肝臓では酸化ストレスが蓄積し、脂質代謝異常が生じますが、これがトリガーになり炎症性細胞が肝臓に集積するという考え方は古くからあります[8, 18]。これに加えて、内臓脂肪組織からの悪玉アディポカインや、腸内細菌叢から門脈を介して伝わるエンドトキシンなどの成分もNAFLからNASHへの移行に影響を与えます[8, 18]。NAFLからNASHへの移行を組織学的に見ると、初期の肝細胞に脂肪滴が観察される脂肪肝、その後、血管周囲から肝実質へ広がる白血球の浸潤(炎症)、肝細胞の空胞変性、さらにはコラーゲン線維の蓄積による線維化(硬化)病変へと進行します。げっ歯類でNAFLDを誘導する際、特に問題となるのは、肝細胞の空胞化や血球の浸潤などNASHに特徴的な肝炎病変をなかなか惹起できない点が挙げられます[10, 15]。そこでNASHに進行させるための様々な工夫がこれまでなされてきました。大きく分けて特殊飼料を給餌させるモデル、特定の遺伝子を改変したモデル、それらの組み合わせモデルが知られています。
2.食餌性NAFLD/NASHモデル
NAFLDは生活習慣病であることから、げっ歯類にも栄養学的に誘導することが試みられました。例えば71%脂質、11%炭水化物、18%のタンパク質からなる高脂肪餌をラットに3週間給餌するとインスリンの効きが悪くなるインスリン抵抗性の誘導と共にNASHの病態を示します[14]。マウスの場合はラットよりNASHを起こしにくいとされ、通常の高脂肪餌の場合1年近くの時間を要することもあります[7]。また、マウスでは食餌性NAFLD誘導における病理変化も比較的弱く、炎症像や線維化像は限定的です。一方で、マウスの場合、系統差が顕著で、例えばC57BL/6系統でもC57BL/6JマウスはC57BL/6Nマウスとくらべて、高脂肪餌給餌後の肝臓へ中性脂肪の蓄積は顕著ですが、肝障害は小さいという報告があります[9]。
洋食に豊富に含まれるコレステロールはヒトでは脂肪性肝炎の主要な原因となります。マウスの場合、1%のコレステロールを給餌するとインスリン抵抗性になりますが、肝重量の増加や血中の脂質量の増加は限定的であり、NASHを含む肝障害には至らないと言われています[14]。一方でコレステロール(例えば1.25%)に一次胆汁酸であるコール酸(例えば0.5%)を加えた餌を与えることもあります。この場合、24週後の肝臓では脂肪の蓄積のみならず肝炎や線維化が認められます[14]。また高コレステロール・コール酸餌に40-75%の中性脂肪を加えることで病状を悪化させることが可能であり、早ければ12週目にはNASHの病態をマウスで観察できます[14]。高コレステロール餌給餌で注意しなければいけないのはコレステロールの量です。1%を超えるコレステロールを与えると、たとえ高脂肪餌を与えても、むしろ内臓脂肪量の減少や体重の減少をもたらすので、ヒトのNASHモデルとは言い難い状態になります[5, 18]。